PET-scanners worden in toenemende mate gebruikt voor diagnostiek, stadiëring en responsmonitoring bij patiënten met kanker. Een nieuwe ontwikkeling hierbij is het gebruik van snelle, digitale detectoren. Potentieel verbetert dit de gevoeligheid, spatiële en temporele resolutie van de PET-scanners. In 2017 zijn in Nederland de eerste digitale PET-scanners geïnstalleerd. Met deze scanners kan de beeldkwaliteit van de PET-scans worden verbeterd, waardoor kleinere laesies beter opgespoord kunnen worden, maar het biedt ook mogelijkheden om de scantijd te verkorten of gebruik te maken van een lagere dosis radioactiviteit.
Leveranciers van digitale PET-scanners wijzen dikwijls op dit laatste aspect, waarbij soms de verwachting wordt gewekt dat dit tevens samengaat met een flinke verbetering in beeldkwaliteit en dus met een verbeterde laesiedetectie. In dit opinieartikel worden de mogelijk- en onmogelijkheden tot verlaging van de dosis dan wel scantijd bij gebruik van een digitale PET-scanner op een rij gezet.
Invloed van tijdsresolutie en spatiële resolutie op PET-beeldkwaliteit
In de afgelopen twee jaar hebben de drie grote fabrikanten van PET-scanners (Siemens, Philips en GE) een digitaal PET-systeem op de markt gebracht. In deze nieuwe apparaten zijn de conventionele detectoren met ‘fotomultipliers’ vervangen door digitale detectoren.
Uiteraard zijn er technische verschillen tussen de digitale PET-scanners van deze drie fabrikanten, maar samengevat biedt digitale PET twee voordelen ten opzichte van conventionele PET: een betere tijdsresolutie (Dt in picoseconde (ps)) en een betere spatiële resolutie (Dr, in mm). Deze factoren hebben beide een effect op de kwaliteit van de PET- beelden.
· Betere tijdsresolutie. Hoe nauwkeuriger het interactietijdstip van een foton in een detector kan worden bepaald, hoe beter time-of-flight (TOF) informatie (het verschil in aankomsttijd tussen twee fotonen van hetzelfde annihilatieproces) gebruikt kan worden in de beeldreconstructie. Een maat voor de effectieve gevoeligheid (Ge) van een PET-scanner kan worden gedefinieerd als de intrinsieke gevoeligheid van het systeem (G, in gemeten counts per seconde per kBq (cps/kBq)) gedeeld door Dt [1]. Bij een gelijkblijvende intrinsieke gevoeligheid impliceert een betere tijdsresolutie (lagere Dt) derhalve de mogelijkheid om de dosis radioactiviteit en/of de scantijd te verlagen, zonder concessies te doen aan de beeldkwaliteit, danwel aan het ruisniveau in de beelden.
· Betere spatiële resolutie. Om te profiteren van de betere intrinsieke spatiële resolutie van een digitale PET-scanner, zodat kleinere laesies beter opgespoord kunnen worden, moet de beeldreconstructie worden aangepast. Dit kan bijvoorbeeld door gebruik te maken van kleinere voxels, door point-spread-function modellering of door minder post-filtering toe te passen in de beeldreconstructie. Hoge resolutie-reconstructies hebben over het algemeen als consequentie dat de ruis in het gereconstrueerde PET-beeld toeneemt. Dit ruisniveau kan zodanig hoog worden dat het een betrouwbare diagnose bemoeilijkt. Een toename in ruis kan gecompenseerd worden door meer counts te verzamelen, door gebruik van een hogere dosis radioactiviteit en/of een langere scantijd.
Van conventionele naar digitale PET
Een reden om over te gaan naar een digitale PET-scanner kan zijn om de diagnostische accuratesse te verbeteren en in het bijzonder de detectie van kleine laesies. Een andere reden kan zijn om de hoeveelheid radioactiviteit en/of scantijd te verlagen, bijvoorbeeld uit kostenoverwegingen, zonder concessies te doen aan de beeldkwaliteit. Uiteraard kunnen ook beide redenen van belang zijn.
Tabel 1 geeft een overzicht van de intrinsieke spatiële resolutie, G, Dt en Ge voor state-of-the-art analoge PET-systemen en de recent geïntroduceerde digitale PET-systemen van de drie grote leveranciers. Er blijken grote verschillen te bestaan in Ge wanneer wordt overgegaan naar een digitaal PET-systeem. Tevens bestaan grote absolute verschillen in effectieve gevoeligheid tussen de leveranciers.
Hoewel de effectieve gevoeligheid een essentiële grootheid is bij de bepaling van de noodzakelijke dosis-scantijd voor een ‘optimale’ beeldkwaliteit, is het niet de enige parameter die een rol speelt. Zo spelen zaken als de scatterfractie, het energie-window waarin fotonen worden geaccepteerd voor verdere processing en de beeldreconstructietechniek ook een rol.
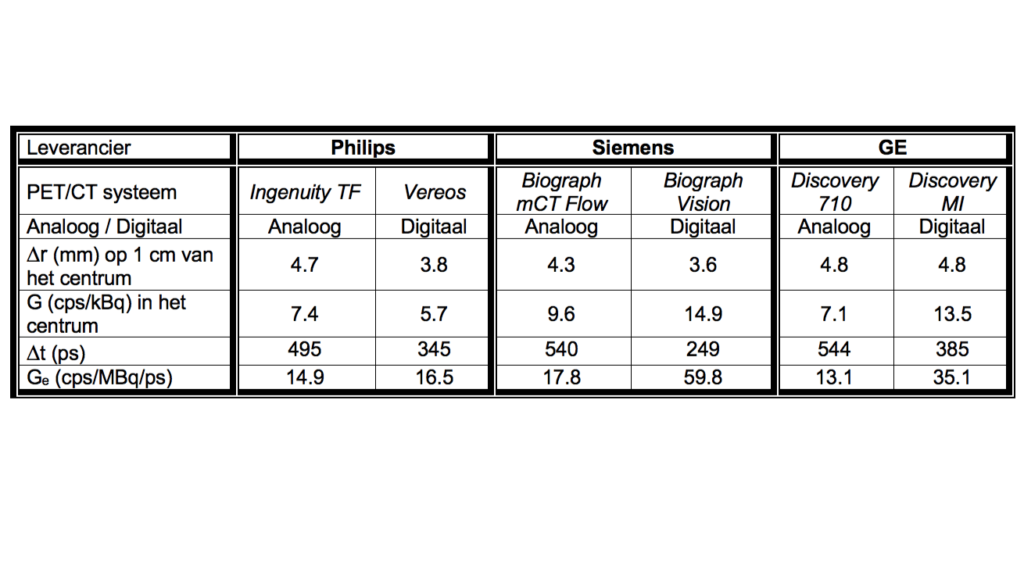
Specificaties van state-of-the-art analoge en digitale PET scanners van Philips, Siemens en GE. De specificaties zijn ontleend aan het artikel van Van der Vos e.a. [2] en voor de Biograph Vision aan de productbrochure van Siemens.
Fantoomstudie
Middels een fantoomstudie kan de relatie tussen ruis en resolutie in de PET-beelden inzichtelijk worden gemaakt. Figuur 1 toont PET-beelden van twee fantomen gevuld met Fluor-18 fluorodeoxyglucose (FDG), waarbij een conventionele PET-scanner (Ingenuity, Philips) en een digitale PET-scanner (Vereos, Philips) zijn vergeleken. We hebben gebruik gemaakt van het NEMA-image quality fantoom (model PET/IEC-BODY-P) met vulbare bollen met diameters variërend van 10 tot 37mm en een microfantoom (model ECT/HS/MMP) met vulbare bollen met diameters van 4 tot 8 mm. Alle fantoombollen zijn gevuld met dezelfde concentratie radioactiviteit en de achtergrond met een 10 keer lagere concentratie. Op beide PET-systemen is een scantijd van 2 minuten gekozen en voor beide systemen is een beeldreconstructie uitgevoerd zodanig dat de best mogelijke beeldresolutie kan worden bereikt. In figuur 1 is te zien dat op de digitale PET-beelden de kleine fantoombollen beter en scherper zichtbaar zijn dan op de conventionele PET-beelden. Echter is tegelijkertijd het ruisniveau bij de digitale PET-beelden ongeveer 20% hoger dan bij de conventionele PET-beelden.
De systeemspecificaties van deze PET-scanners (Tabel 1) laten zien dat G=7,4 en 5,7 cps/kBq, voor de conventionele, respectievelijk digitale PET-scanners. De tijdsresolutie van de systemen is 495, respectievelijk 345 ps. Ofwel, de lagere gevoeligheid G van het digitale systeem wordt gecompenseerd door de hogere tijdsresolutie. Daardoor is de effectieve gevoeligheid Ge voor het digitale systeem uiteindelijk 11% hoger dan die van het conventionele systeem. Vanwege dit beperkte verschil kan worden gesteld dat de fantoomstudie laat zien dat het ruisniveau direct gerelateerd is aan de beeldresolutie: een betere beeldresolutie gaat gepaard met een hoger ruisniveau. Zouden we een gelijkblijvend ruisniveau wensen bij het digitale systeem, zonder concessies te doen aan de maximaal haalbare beeldresolutie, dan dient de gebruikte dosis radioactiviteit en/of de scantijd te worden verhoogd.

Optimaal gereconstrueerde FDG-PET-beelden vaneen NEMA-image quality fantoom (bol diameters 10-37 mm) en een microfantoom (bol diameters 4-8 mm) gescand op een conventionele PET (links) en een digitale PET (rechts). Op de digitale PET-beelden zijn de (kleine) bollen scherper en duidelijker zichtbaar. Tegelijkertijd is het ruisniveau wel toegenomen.
Klinische illustratie
Figuur 2 toont een digitale PET-scan van een patiënt met een aantal FDG-positieve afwijkingen. Het gebruik van kleinere voxels, zoals getoond in figuur 2B en 2C, leidt tot een hogere beeldresolutie en daarmee tot een betere zichtbaarheid van kleine afwijkingen. Dit heeft echter ook tot gevolg dat de ruis in het beeld toeneemt bij gebruik van eenzelfde dosis en scantijd. Dit kan de beoordeling van de scan bemoeilijken en leiden tot fout-positieve resultaten.
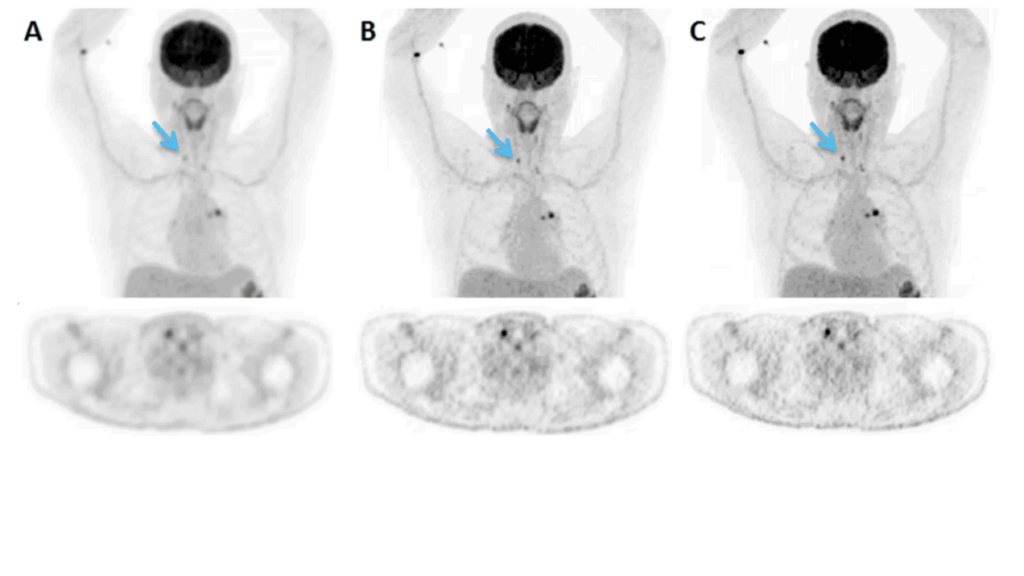
Coronale (boven) en transversale (onder) digitale PET-beelden (Vereos, Philips) van een patiënt met meerdere FDG-positieve afwijkingen. A. reconstructie met 4x4x4 mm3voxels (normale-resolutie reconstructie). B: reconstructie met 2x2x2 mm3voxels (hoge-resolutie reconstructie). C: reconstructie met 1x1x1 mm3voxels (ultra-hoge-resolutie reconstructie). De zichtbaarheid van de laesie in de hals neemt duidelijk toe met gebruik van de reconstructie met hogere resolutie. De ruis in de beelden neemt echter ook toe.
Conclusie
Digitale PET-scanners beschikken over een potentieel betere tijdsresolutie en spatiële resolutie. Deze eigenschappen kunnen gebruikt worden om kleine laesies beter op te sporen, maar bieden ook de mogelijkheid om de scantijd van een PET-onderzoek te verkorten of een lagere dosis radioactiviteit toe te passen. Het is echter niet reëel om de hoogst haalbare beeldresolutie met een digitale PET-scanner te combineren met de laagst haalbare dosis activiteit en/of scantijd, omdat beide een tegengesteld effect hebben op het ruisniveau in de gereconstrueerde PET-beelden. Om inzicht te krijgen in de mogelijkheden en onmogelijkheden van een digitale PET-scanner, is kennis van de effectieve gevoeligheid van het systeem in combinatie met de haalbare beeldresolutie van belang. Uiteindelijk dient de gebruiker van een digitaal PET-systeem een keuze te maken tussen het maximaliseren van de beeldkwaliteit enerzijds en het verlagen van de dosis en/of scantijd anderzijds.
Auteurs
Daniëlle Koopman (technisch geneeskundige), Piet Jager (nucleair geneeskundige) en Jorn van Dalen (klinisch fysicus)
Referenties
[1] Karp, Joel S., et al. The benefit of time-of-flight in PET imaging: Experimental and clinical results.” Journal of nuclear medicine: official publication, Society of Nuclear Medicine49.3 (2008): 462-470.
[2] van der Vos, Charlotte S., et al. “Quantification, improvement, and harmonization of small lesion detection with state-of-the-art PET.” European journal of nuclear medicine and molecular imaging 44.1 (2017): 4-16