Geraffineerde onderzoekstechnieken maken het mogelijk dat het gehoor nauwkeurig en betrouwbaar in zeer korte tijd objectief onderzocht kan worden. Een tweetal methoden zijn de afgelopen jaren ontwikkeld: het meten van oto-akoestische emissies (dit zijn opgewekte geluiden die als het ware uit het oor lijken te komen) en de geautomatiseerde auditieve hersenstam respons.
Inleiding
Beide methoden worden inmiddels veelvuldig toegepast en zijn zowel qua sensitiviteit als specificiteit, maar ook qua betrouwbaarheid, beter dan de niet objectieve Ewing-test.
Als de resultaten van dit nieuwe onderzoek daartoe aanleiding geven, dan kan nog preciezer objectief gehooronderzoek plaatsvinden, in de vorm van auditief hersenstamonderzoek of elektrocochleografie. De uitkomsten van deze beide onderzoekingen (“gouden standaard”) geven een heel precieze indicatie (nauwkeurigheid 5 dB) van het gehoorverlies, waarbij elektrocochleografie heel strikt differentieert naar de frequentie van de aangeboden tonen. Bovendien wordt elektrocochleografie toegepast bij kandidaten voor cochleaire implantatie en bij verdenking op Morbus Ménière.
Ontwikkeling van het gehoororgaan vanaf de conceptie
Binnen een maand na de conceptie zijn al de eerste contouren van de aanleg van de cochlea te zien. Een maand later volgen de drie half cirkelvormige kanalen die het evenwichtsorgaan gaan vormen. Op de derde maand krijgt het middenoor al vorm door de aanleg van de middenoor gehoorbeentjes: hamer, aambeeld en stijgbeugel.
De gehoorzenuw begint op de vijfde maand te functioneren en niet veel later is de waarnemingsfunctie in de hersenen in orde. Dat weten we omdat prematuur geboren baby’s van 25 weken op geluid kunnen reageren en omdat op die leeftijd auditieve hersenstam re-sponsen gemeten kunnen worden. Bij de geboorte is de cochlea al even groot als die van een volwassene. Het middenoor groeit ook nauwelijks meer. Maar de rijping van de gehoorzenuw laat nog even op zich wachten, uiteindelijk duurt dat tot bijna vijftienjarige leeftijd.
Oorzaken van slechthorendheid, risicofactoren
Heel globaal kan slechthorendheid het gevolg zijn van al dan niet aangeboren (syndromaal of non-syndromaal) of zowel pré-, peri- als postnataal verworven middenoor- en binnenoorafwijkingen. Bovendien kunnen we nog auditieve neuropathie onderscheiden (komt zelden voor, meestal pas op latere leeftijd), zoals neurofibromatose en (multipele) sclerose. Uit een studie van Van Rijn (1989) blijkt dat bij 40% van alle slechthorende kinderen sprake is van erfelijke factoren, waarvan ruim de helft autosomaal recessief (met daarbij congenitale anomalieën, vaak syndromale afwijkingen).
Bijna een derde van de slechthorende kinderen heeft verworven slechthorendheid, door prenatale in-fecties (bijv. rubella en syfilis), perinatale infecties (vooral geelzucht), postnatale infecties (zoals hersenvliesontsteking en mazelen) of ototoxische medicatie, bij ruim een derde van de slechthorende kinderen is geen oorzaak bekend.
Bij de ziekste kinderen met een sterk verhoogd risico (geboren op de neonatale intensive care units) zijn de risico factoren: laag geboortegewicht (minder dan 1500 g), zeer vroeg geboren (jonger dan 32 weken zwangerschapsduur) en stoornissen in vitale levensfuncties.
Gehooronderzoek
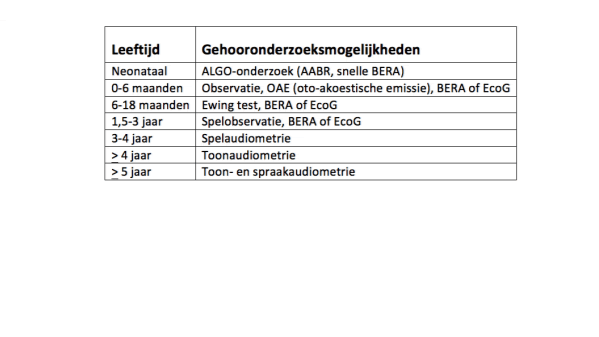
In tabel 1 staat een schematisch overzicht welk gehooronderzoek op welke leeftijd opportuun is.
Uit gegevens van TNO (1995) komen de volgende prevalentiecijfers naar voren: slechthorendheid komt bij 4,5% tot 11,4% van de Nederlandse bevolking voor, dat betreft voornamelijk ouderen. Bij kinderen (audiometrie bij schoolkinderen) wordt bij gemiddeld 3% een gehoorverlies van minstens 30 dB gemeten (inclusief OME). Uit het verleden weten we dat bij 1‰ van alle pasgeborenen ernstige perceptieve slechthorendheid voorkomt, in Nederland betreft dat zo’n 200 baby’s per ruim 200.000 geboortes per jaar.
De afgelopen jaren is men het wereldwijd erover eens geworden dat opsporing van slechthorendheid op zo jong mogelijke leeftijd (vóór 6 maanden) dient plaats te vinden, om ervoor te zorgen dat de spraak-, taal- en gehoorontwikkeling van deze risicokinderen zo goed mogelijk kan verlopen door toepassing van de nodige hulpmiddelen (hoortoestellen) en adequate opvang, zoals hoor?, spraak- en taaltraining en gezinsbegeleiding. De effecten zijn opzienbarend (Yoshinaga, 1998). Waar voorheen ernstig slechthorende kinderen jarenlang het speciaal onderwijs moesten volgen stromen ze nu al steeds vaker vanaf 4 jaar het reguliere onderwijs in.
Geautomatiseerde auditieve hersenstam respons
Het doel van dit onderzoek is het bepalen van de gehoorfunctie van middenoor, via binnenoor tot de auditieve zenuwbanen in de hersenstam.
Bij de normale hersenstamaudiometrie (BERA = Brainstem Electric Response Audiometry) wordt een kortdurende geluidsstimulus via een hoofdtelefoon 10 – 20 maal per seconde aan het oor aangeboden. Als het middenoor en het binnenoor goed functioneren ontstaat in reactie hierop synchroon activiteit in een groot aantal vezels van de gehoorzenuw. Door de stimulus honderden keren aan te bieden en even vaak de zenuwrespons te meten, op te tellen en te middelen, kan het ontstane patroon tot vlak boven de gehoordrempel opgetekend worden, verschillend van de achtergrondruis, waardoor nauwkeurig de objectieve gehoordrempel bepaald kan worden. Het onderzoek kan onder en vaak ook zonder sedatie worden uitgevoerd en leent zich daarom goed voor gehooronderzoek bij kinderen.
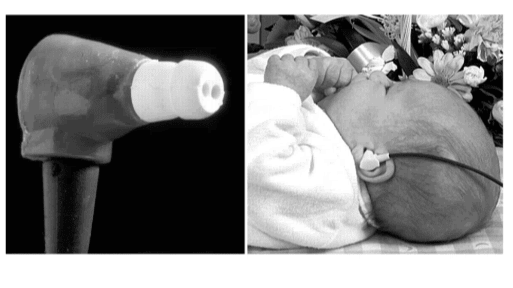
De AABR (Automatic Auditory Brainstem Response), ook screenings-BERA genoemd, test het gehoor van beide oren bij 50, 40 en 30 dB(nHL). De meting duurt kort en kan daarom veelal zonder anesthesie worden verricht, maar bij voorkeur wel bij een rustend persoon of een slapend kind. Wordt een reactie gevonden dan is dit een hard gegeven, en een betrouwbare reactie bij 30 dB(nHL) wordt gezien als aanduiding voor voldoende gehoor, waarbij sensitiviteit en specificiteit beter zijn dan 97%, mits goed uitgevoerd (geen sinecure). Het apparaat geeft een eenduidige uitslag.
Bij het ontbreken van een respons bij deze intensiteiten is nader onderzoek nodig (CvZ, 2000), omdat deze methode geen informatie verschaft over de aard en de gradatie van gehoorverlies.
Oto-akoestische emissies (OAE’s)
Het doel van het objectieve gehooronderzoek met OAE’s is de beoordeling van de gevoeligheid van het oor voor geluid: van gehoorgang tot en met de haarcellen in het binnenoor.
Het fenomeen Oto Akoestische Emissie (OAE) is sinds 1978 bekend. Een gezond oor kan geluid produceren tijdens en kort na stimulatie. Aanvankelijk dacht de ontdekker van dit verschijnsel, prof. Kemp uit London, dat dit geluidje een reflectie was van het aangeboden geluid. Maar later bleek dat het een resonantie is van de mechanische activiteit van de buitenste haarcelen in het binnenoor. De OAE is een zwak geluidje en kan worden geregistreerd met een microfoontje, dat is gemonteerd in een dopje dat in de opening van de gehoorgang wordt aangebracht. In datzelfde dopje is ook een telefoontje aanwezig om het oor met geluid te kunnen stimuleren. Het fenomeen is préneuraal. Als een OAE kan worden geregistreerd bewijst dat een (vrijwel) goede functie van het binnenoor en het middenoor (geen OME, geen afsluitende cerumenprop), maar het bewijst strikt genomen niet dat de patiënt met dat oor ook normaal kan horen, daar er een centrale gehoorafwijking zou kunnen zijn die normaal horen verhindert. In de praktijk wordt OAE onderzoek als afdoende gehoorscreening beschouwd, omdat centrale slechthorendheid zeer zeldzaam is, meestal gepaard gaande met andere aandoeningen (meestal syndromen, bijvoorbeeld Morbus Recklinghausen, multiple sclerose, etc.).
Behalve voor het nauwkeurig en frequentie specifiek bepalen van de gehoordrempel bij hele jonge kinderen wordt ECoG onderzoek toegepast bij zeer ernstig slechthorende en dove kinderen en volwassenen die in aanmerking komen voor een cochleair implantaat, en bij slechthorende volwassenen met een verdenking op of ter uitsluiting van Morbus Ménière of Morbus Lermoyez of soortgelijke cochleaire stoornissen, dan wel andere onbegrepen cochleaire gehoorafwijkingen.
Bij (zeer) jonge kinderen is de vraagstelling gericht op de cochleaire gehoordrempel. Een drempelwaarde wordt bereikt zodra de beschreven responsen bij afnemende intensiteit van de stimulus in de ruis verdwijnen (zoals bij het BERA onderzoek, zie vorige figuur). Een elektrocochleogram brengt bij de octaaf- en desgewenst tussenliggende frequenties van 500 Hz tot 8000 Hz het objectieve audiogram in kaart, opgetekend voor beide oren. Het gaat meestal om het bepalen van het restgehoor van het ernstig slechthorende kind, waardoor optimale stimulatie met gehoorapparatuur of cochleaire implantaten mogelijk gemaakt kan worden.
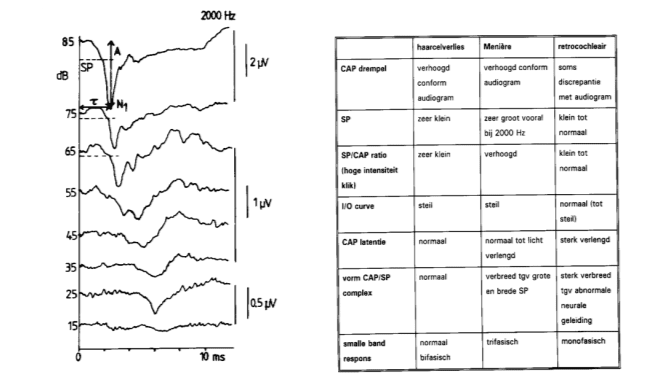
Bij volwassenen wordt vaak bij één oor en soms beiderzijds onderzoek gedaan. Niet alleen het objectieve audiogram is dan van belang, maar ook het fysiologisch functioneren van het binnenoor is te analyseren. Abnormaal steile input-outputcurven waarin latentie en amplitude van de actiepotentiaal uitgezet zijn tegen de intensiteit van de aangeboden stimulus passen bij het beeld van loudness recruitment (cochleair). Een vergrote sommatie potentiaal (in vergelijking met de samengestelde actiepotentiaal) wijst op de ziekte van Ménière en de afwezigheid van de sommatiepotentiaal duidt op haarcel laesies. Een andere afwijking bij de ziekte van Ménière betreft de meestal trifasische golfvorm van de smalle band respons (tegenover bifasisch normaal). Verlengde latenties kunnen soms wijzen op retrocochleaire stoornissen (zoals het geval is bij verlengde intertoplatenties van hersenstam responsen).
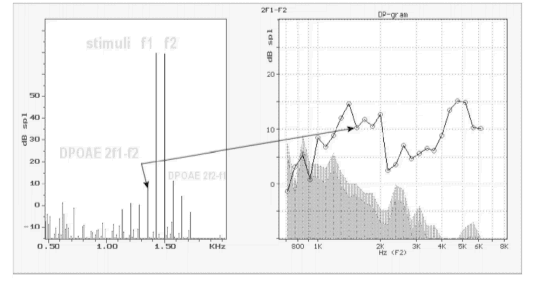
OAE’s worden geregistreerd tijdens of kort na stimulatie van het te onderzoeken oor. Het registreren van de zwakke emissie in aanwezigheid van de veel sterkere stimulus is technisch lastig, maar goed opgelost voor twee stimuluscondities. De meest gebruikte stimulus is een korte klikstimulus (< 10 µsec) daarmee worden de Transient Evoked Oto Acoustic Emissions (TEOAE) gemeten. De andere klinisch bruikbare stimulus is een complex van twee zuivere tonen (de primaire tonen). Een goed functionerend oor genereert door vervorming tijdens het verwerken van deze stimulus extra tonen. Deze soort heet dan ook Distortion Product Oto Acoustic Emissions (DPOAE). Vervormingsprodukt oto-akoestische emissies worden opgewekt door de niet-lineariteit in de elektro-mechanische en mechano-elektrische transductie in de buitenste haarcellen, met andere woorden: de buitenste haarcellen in het binnenoor lijken te resoneren zodra er twee tonen aangeboden worden die niet veel van elkaar verschillen qua toonhoogte en qua geluidniveau. Anders dan bij de klik-opgewekte emissies worden bij deze methode twee lange tonen aangeboden waarna men een door het binnenoor veroorzaakte derde toon (emissie) in de gehoorgang kan meten. Doordat deze emissie van een klein gebied in de cochlea afkomstig is kan met deze vervormingsprodukt-emissies frequentie-specifiek gehoorbeschadiging opgespoord worden.
Door meettechnische beperkingen is het klinisch te testen bereik van de OAE’s in de regel beperkt van 1 – 6 kHz. Op dit moment is er geen duidelijk argument om te kiezen voor het registreren van TEOAE’s of DPOAE’s. Beide hebben klinisch evenveel waarde.
Aanwezigheid van oto akoestische emissies bij een bepaalde toonhoogte bewijst dat het onderzochte oor geen gehoorverlies groter dan 25-35 dB kan hebben voor die toonhoogte. Afwezigheid maakt een disfunctie van het oor bij die toonhoogte waarschijnlijk. In de algemene populatie is de specificiteit voor het vaststellen dat een oor (vrijwel) normaal gevoelig is meer dan 97%. Dit maakt de OAE meting zo geschikt als gehoor screening. Ook de sensitiviteit voor gevoeligheidsverliezen van meer dan 35 dB is meer dan 97%.
Hersenstamaudiometrie
Herstamaudiometrie is elektro-audiometrisch onderzoek, dat toegepast wordt om de gehoorfunctie te onderzoeken en om de geleidingstijden van de auditieve banen in de hersenstam te bepalen in het kader van vroegdiagnostiek van otoneurologische aandoeningen, waaronder gezwellen in de brughoek (retrocochleair).
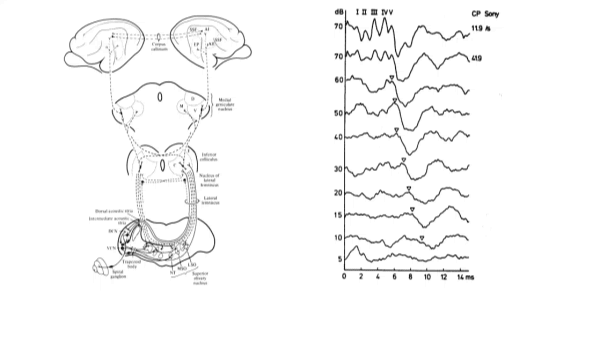
Vóór het onderzoek moet het uitwendige oor worden geïnspecteerd. In geval van afsluiting van de gehoorgang moet deze eerst worden vrijgemaakt. Bij hersenstam audiometrie (BERA = Brainstem Electric Response Audiometry) wordt een kortdurende geluidstimulus via een hoofdtelefoon of bij uitzondering een luidspreker 10 – 20 maal per seconde aan het oor aangeboden. In reactie hierop ontstaat synchroon activiteit in een groot aantal vezels van de gehoorzenuw. Hierop volgt een kettingreactie, waarbij respectievelijk de nucleus cochlearis, de oliva superior, de laterale lemniscus en de colliculus inferior elektrische potentialen produceren. Het gelijktijdig vuren van de zenuwvezels resulteert in de “samengestelde actiepotentiaal”. Dit is een optelling van de activiteit in de afzonderlijke zenuwvezels. Deze samengestelde actiepotentiaal wordt geregistreerd met een elektrode op de vertex. Eventueel kan een ander punt op de schedel worden gekozen op de lijn vertex – nasion.
Achter het te onderzoeken oor wordt een elektrode op het mastoïd geplaatst en achter het contralaterale oor een referentie elektrode als aardelektrode. Doordat het geluid herhaald wordt aangeboden kan de samengestelde actiepotentiaal een groot aantal malen worden gemeten (1000 – 4000 maal). Dit maakt het mogelijk de samengestelde actiepotentiaal met een middelingsprocedure uit de ruis te filteren. De respons die tenslotte wordt gevonden, is een middeling van een groot aantal metingen van de samengestelde actiepotentialen. De meting bestaat uit een vijftal toppen, respectievelijk ongeveer 1,5 – 2,5 -3,5 – 4,9 en 7,0 msec na de stimulus ontstaan. De laagste intensiteit waarbij een respons wordt gezien, is een maat voor het gehoorverlies tussen 2 – 4 kHz.
Bij een groot aantal aandoeningen van de auditieve banen in de hersenstam ontstaan de verschillende toppen later dan normaal. Bij 10% latentieverlenging (of meer) wordt uitsluitende beeldvormende diagnostiek aanbevolen. Het onderzoek kan worden uitgevoerd bij een rustend persoon, bijvoorbeeld een slapend kind, indien nodig onder sedatie.
Elektrocochleografie
Elektrocochleografie is een bijzondere vorm van elektro-audiometrie, die enerzijds toegepast wordt om zo nauwkeurig mogelijk en objectief, frequentie specifiek de cochleaire gehoordrempel te bepalen als dat subjectief niet mogelijk is, en die anderzijds toegepast wordt om bijzondere cochleaire en neurale gehoorfunctiestoornissen fysiologisch te interpreteren.
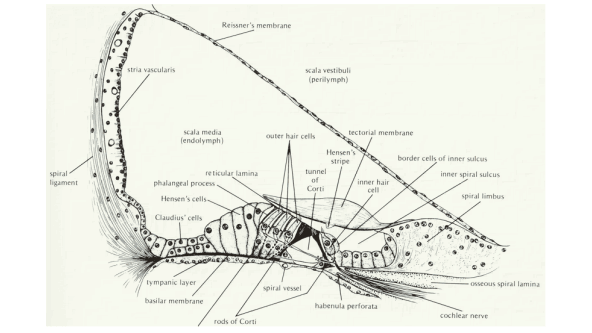
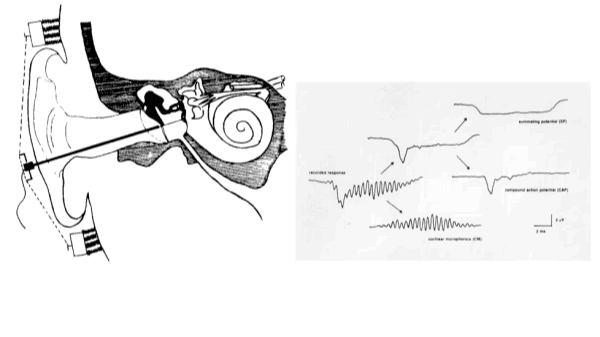
De fysiologische responsen van het binnenoor worden gemeten met een elektrode die zich bij voorkeur zo dicht mogelijk in de nabijheid van de cochlea bevindt, zoals een op het promontorium geplaatste transtympanale naald elektrode. Daarom wordt het onderzoek bij volwassenen gedaan met plaatselijke verdoving (in de gehoorgang) en bij kinderen onder lichte narcose. De tweede elektrode is op het mastoïd geplaatst en de aardelektrode op het voorhoofd. Als stimuli worden clicks of korte toonstoten met frequenties van 500 Hz tot 8000 Hz gebruikt. De responsen hebben amplituden in het 0.1-10 mV bereik. Ze worden versterkt, gefilterd en 500 maal opgeteld en gemiddeld om de signaal-ruis verhouding te verbeteren. Met toon stoten verkrijgt men op directe wijze informatie over het functioneren van juist dat frequentiegebied van de cochlea dat specifiek voor de betreffende stimulusfrequentie gevoelig is.
Met andere woorden: er bestaat een tonotopische relatie tussen de frequentie van de aangeboden toonstimulus en het cochleaire activatiepatroon. De respons bestaat uit drie componenten. De cochleaire microfonie is afkomstig van de buitenste haarcellen en vormt een afspiegeling van de door de stimulus veroorzaakte oscillatie van het basilair membraan. Deze potentiaal heeft geen diagnostische waarde en wordt meestal geëlimineerd door de stimuli met alternerende polariteit aan te bieden. De tweede component, de sommatiepotentiaal is ook afkomstig van vooral de buitenste haarcellen. Het is een gelijkspanningspotentiaal die optreedt gedurende de stimulus en is een uiting van niet-lineariteit in de cochleaire transductie. De derde component is de samengestelde actiepotentiaal van de gehoorzenuw, die het resultaat is van het synchroon vuren van een aantal vezels van de gehoorzenuw op het begin van de toonstoot.
Behalve voor het nauwkeurig en frequentie specifiek bepalen van de gehoordrempel bij hele jonge kinderen wordt ECoG onderzoek toegepast bij zeer ernstig slechthorende en dove kinderen en volwassenen die in aanmerking komen voor een cochleair implantaat, en bij slechthorende volwassenen met een verdenking op of ter uitsluiting van Morbus Ménière of Morbus Lermoyez of soortgelijke cochleaire stoornissen, dan wel andere onbegrepen cochleaire gehoorafwijkingen.
Bij (zeer) jonge kinderen is de vraagstelling gericht op de cochleaire gehoordrempel. Een drempelwaarde wordt bereikt zodra de beschreven responsen bij afnemende intensiteit van de stimulus in de ruis verdwijnen (zoals bij het BERA onderzoek, zie vorige figuur). Een elektrocochleogram brengt bij de octaaf- en desgewenst tussenliggende frequenties van 500 Hz tot 8000 Hz het objectieve audiogram in kaart, opgetekend voor beide oren. Het gaat meestal om het bepalen van het restgehoor van het ernstig slechthorende kind, waardoor optimale stimulatie met gehoorapparatuur of cochleaire implantaten mogelijk gemaakt kan worden.
Bij volwassenen wordt vaak bij één oor en soms beiderzijds onderzoek gedaan. Niet alleen het objectieve audiogram is dan van belang, maar ook het fysiologisch functioneren van het binnenoor is te analyseren. Abnormaal steile input-outputcurven waarin latentie en amplitude van de actiepotentiaal uitgezet zijn tegen de intensiteit van de aangeboden stimulus passen bij het beeld van loudness recruitment (cochleair). Een vergrote sommatie potentiaal (in vergelijking met de samengestelde actiepotentiaal) wijst op de ziekte van Ménière en de afwezigheid van de sommatiepotentiaal duidt op haarcel laesies. Een andere afwijking bij de ziekte van Ménière betreft de meestal trifasische golfvorm van de smalle band respons (tegenover bifasisch normaal). Verlengde latenties kunnen soms wijzen op retrocochleaire stoornissen (zoals het geval is bij verlengde intertoplatenties van hersenstam responsen).
Referenties
[1] AMJ Chorus et al, Slechthorendheid in Nederland, TNO-rapport 95.076. 1995, Leiden.
[2] College van Zorgverzekeringen (2000). Diagnostisch Compas 2000-2001. Amstelveen.
[3] De Laat JAPM, Eekhof JAH (2003). Nieuwe ontwikkelingen bij onderzoek en revalidatie van gehoorverlies. In: Vorderingen en Praktijk, Boerhaave Cursus voor Huisartsen. Redactie: Bolk JH, et al. Cursusboek Boerhaave Commissie, LUMC, Leiden, 223-233.
[4] Dornhoffer JL (1998). Diagnosis of cochlear Meniere’s disease with elektrocochleography. ORL J Otorhinolaryngol Relat Spec; 60(6): 301-5.
[5] Eekhof JAH, De Laat JAPM (2002). Slechter horen. Huisarts en Wetenschap; 45 (12): 689-693.
[6] Eggermont JJ, Odenthal DW, Schmidt PH, et al. (1974). Elektrocochleography. Basic Principles and clinical application. Acta Otolaryngol; Suppl 316: 1-84.
[7] Hall JW (1992). Handbook of auditory evoked responses. Needham Heights, Mass: Allyn & Bacon.
[8] Kemp DT (1978). Stimulated acoustic emissions from within the human auditory system. J Acoust Soc Am, 64, 1368-1391.
[9] Olphen AF van (1983). Auditieve hersenstam potentialen bij de mens. Dissertatie. Erasmus Universiteit Rotterdam.
[10] Prijs VF (1993). Emissies door vervorming als test voor een goed gehoor. In: Schoonhoven, Grote, Prijs, De Laat: Objectieve audiometrie. Cursusboek Boerhaave Commissie, Leiden, 99-116.
[11] MS Robinette et al, Otoacoustic Emissions: Clinical Applications. New York, 1993, Thieme.
[12] M Rodenburg et al, Audiometrie: methoden en klinische toepassingen. 1998, Muiderberg: Coutinho.
[13] R Schoonhoven et al, Objectieve audiometrie. Cursusboek Boerhaave commissie, 1993, LUMC, Leiden.
[14] Van Rijn PM (1989). Causes of early childhood deafness. Dissertatie. Katholieke Universiteit Nijmegen.
[15] Van Straaten I (2001). Automated auditory brainstem response hearing screening in NICU graduates. Dissertatie. Universiteit van Amsterdam.
[16] C Yoshinaga-Itano et al, Language of early- and later-identified children with hearing loss. Pedriatrics, 102, 1998, pp.1161-1171.