Photodynamische Therapie, afgekort PDT, is een behandelmethode waarbij tumoren lichtgevoelig worden gemaakt en daarna met laserlicht worden belicht zodat deze afsterven. Deze behandeling wordt in het Antoni van Leeuwenhoek (AvL) te Amsterdam al sinds 1996 klinisch toegepast voor primair en recidief plaveiselcelkanker in het hoofd hals gebied. De belichtingen vinden meestal plaats in de mond- en keelholte, veel voorkomende doelgebieden zijn: tong, wangslijmvlies, mondbodem, palatum en lip. Maar ook ernstige dysplasie in de mondholte kan met PDT worden behandeld.
Over PDT
Bij deze behandelmethode wordt gebruik gemaakt van een lichtgevoelige stof, photosensitizer, en van laserlicht met een bepaalde golflengte. Allereerst wordt bij de patiënt de photosensitizer langzaam in een grote perifere vene ingespoten en deze verdeeld zich dan door het gehele lichaam. De patiënt is dus vanaf dat moment gevoelig voor licht. De inspuiting van de photosensitizer gebeurt bij de patiënt thuis door een verpleegkundige van de thuiszorgorganisatie Medihands. Vier dagen later wordt de tumor in het ziekenhuis belicht met laserlicht met een golflengte van 652 nm (rood licht).
Door de combinatie van photosensitizer, licht en zuurstof, dat aanwezig is in het bloed, zorgt dit voor een non-thermische fotochemische reactie wat leidt tot tumor necrose. Dit wordt veroorzaakt doordat de photosensitizer geactiveerd wordt door het laserlicht met deze specifieke golflengte waardoor zeer actieve vrije zuurstofradicalen worden gevormd. Deze vrije zuurstofradicalen gaan interacties aan met de cel waardoor deze stuk gaat. De lifetime van de geproduceerde zuurstofradicalen is zeer kort, waardoor de reikwijdte ongeveer 10-55 nm in de cellen is. Het type schade aan de cel is dus afhankelijk van waar de photosensitizer zich in de cel bevind. Elke type photosensitizer heeft een verschillende verblijflocatie in de cel.
Als photosensitizer wordt gebruik gemaakt van Foscan® (m-tetrahydroxyphenylchlorin, mTHPC), de werkzame stof is temoporfine. Temoporfine is een zogenaamde tweede generatie photosensitizer. De eerste generatie photosensitizers, zoals Photofrin, hadden nogal wat bijwerkingen zoals, hoge fototoxiciteit (waardoor patiënten maandenlang niet in het licht mochten komen), de lange belichtingstijd (20 tot 30 minuten) en de geringe penetratiediepte in weefsel (5 mm). Temoporfine heeft minder bijwerkingen, een korte belichtingstijd van 200 seconden en heeft een grotere penetratiediepte van 10 mm. De schade die aan de cel wordt veroorzaakt door de Foscan, wordt voornamelijk veroorzaakt door schade aan de mitochondriën en het endoplasmatisch reticulum. De concentratie Foscan die wordt toegediend bedraagt 0.15 mg / kg lichaamsgewicht.
Lichtgevoelig
Dat patiënten lichtgevoelig zijn na de inspuiting van Foscan betekent niet dat ze niet in het licht mogen komen. Patiënten krijgen een licht opbouwschema mee en een luxmeter, op de dag van inspuiting mogen ze in een ruimte bevinden van maximaal 100 lux wat overeenkomt met een gloeilamp van 60W (spaarlamp van 11W). Elke dag mag de lichtsterkte met 100 lux worden verhoogd, na vier dagen (de dag van behandeling) mogen ze maximaal 500 lux hebben wat overeenkomt met kantoorverlichting. Dus beperkte binnenhuis verlichting en verlichting van televisie en computerschermen zijn normaliter veilig, ook direct na inspuiting.
Echter de eerste twee weken moet direct daglicht worden vermeden dus als mensen naar buiten moeten, moeten ze helemaal zijn bedekt, ook het gezicht. Blootstelling aan een te grote lichtsterkte kan leiden tot ernstige verbranding van de huid. Na twee weken mag stapsgewijs de huid worden blootgesteld aan daglicht. Het is belangrijk om goed aan het licht opbouwschema te houden, omdat Foscan juist door licht wordt afgebroken en niet door het lichaam zelf. Na drie maanden zijn er geen beperkingen meer.
Voordelen
De grote voordelen van PDT zijn:
- Kortdurende, eenmalige behandeling
- Nauwkeurig toe te passen, waardoor er minder snel sprake is van functieverlies van het behandelend gebied.
- Inzetbaar na eerdere chirurgische of radiotherapeutische behandelingen of een eerdere behandeling met PDT.
- Ziekenhuisopname beperkt, meestal binnen twee dagen weer thuis.
Wel is de behandeling met PDT de eerste 6 tot 8 weken pijnlijk door zwelling en necrose van het behandelend gebied. Standaard wordt er gerichte pijnmedicatie gegeven en medicatie om de zwelling te verminderen. De intensiteit van de bijwerkingen zijn ook weer afhankelijk van het behandelende gebied en de uitgebreidheid van de tumor.
Het is belangrijk om de patiënt vooraf goed te informeren en voor te bereiden en na de behandeling goed te blijven monitoren. Zo worden patiënten de eerste maand na de behandeling die uit het ziekenhuis ontslagen zijn meerdere keren per week gebeld door de verpleegkundige om te horen hoe het gaat met o.a. de pijn, zwelling en lichtbelasting. Eventueel kan dan de medicatie hiervoor worden aangepast.
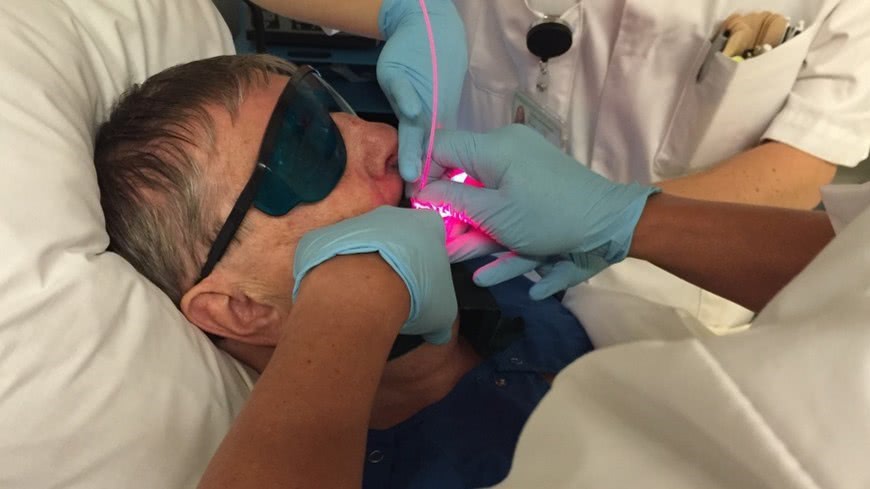
Methode
De meeste PDT behandelingen gebeuren onder algehele narcose op de OK, voor makkelijk te bereikbare doelgebieden, zoals lip, kan dit ook worden gedaan onder plaatselijke verdoving. De belichting van het doelgebied kan op drie manieren worden gedaan: oppervlakkig, interstitieel of intraluminair.
Oppervlakkige belichting wordt gedaan bij tumoren met een maximale dikte van 4 mm. De belichting gebeurt met een microlens fiber die, afhankelijk van de grote van het behandelend oppervlak, op een bepaalde afstand wordt gehouden. Het laserlicht heeft een penetratiediepte van 10 mm. Het doelgebied wordt belicht met een marge van 5 mm rondom de tumor, gezond weefsel wordt afgeschermd met natte groene doeken en/of zwarte wax. De afgegeven energie van het laserlicht aan de tumor bedraagt voor deze behandelingen (met uitzondering van de interstitiële PDT) 20 J/cm2. De fluence rate van de laser bedraagt 100 mW/cm2 wat dus resulteert in een belichtingstijd van 200 s.
Alternatieve belichting
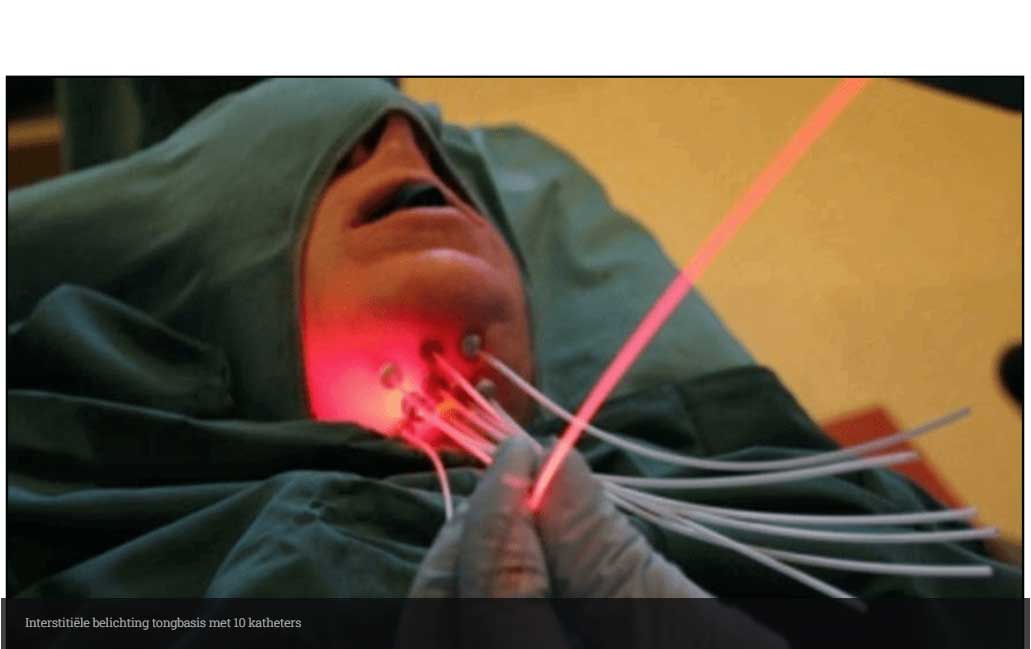
Als de tumor dikker is dan 4 mm of dieper gelegen is waardoor oppervlakkige belichting niet mogelijk is, kan de belichting in bepaalde gevallen interstitieel gedaan worden. Hiervoor worden lichtdoorlatende kunststof katheters of naalden in het doelgebied geïmplanteerd. In deze kunststof katheters of naalden gaat een lichtfiber en wordt de tumor van “binnenuit” belicht.
Een toepassing van interstitiële PDT, is de belichting van recidief tongbasiscarcinomen. Deze groep patiënten hebben meestal PDT als laatste behandeloptie, omdat zij in het verleden vaak al uitvoerig zijn behandeld waardoor chirurgie en (her)bestraling niet meer mogelijk zijn. De dosis voor deze behandeling is 30 J/cm met een belichtingstijd van 300 s.
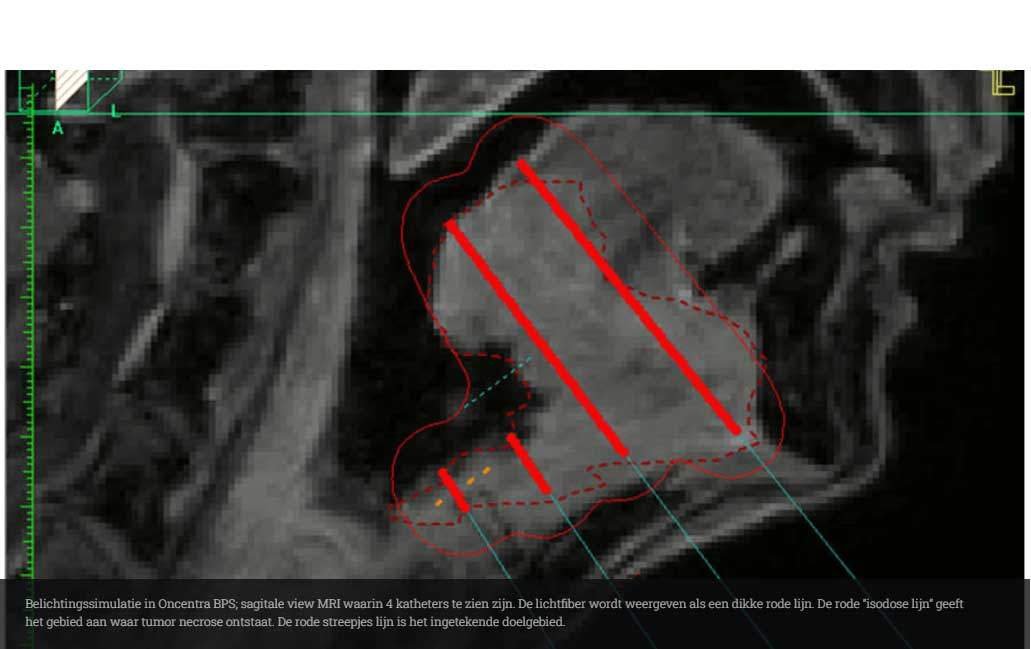
Voor deze behandeling wordt vooraf een “belichtingsplan” gemaakt, hiervoor wordt een MRI gemaakt waarop het doelgebied wordt ingetekend door de radiotherapeut en hoofd-hals chirurg. Vervolgens wordt in het Oncentra brachyplanningssysteem (BPS), op de ingetekende MRI, katheters gepland en worden de lichtfibers gesimuleerd door “lichtbronnetjes” in de katheters aan te zetten.
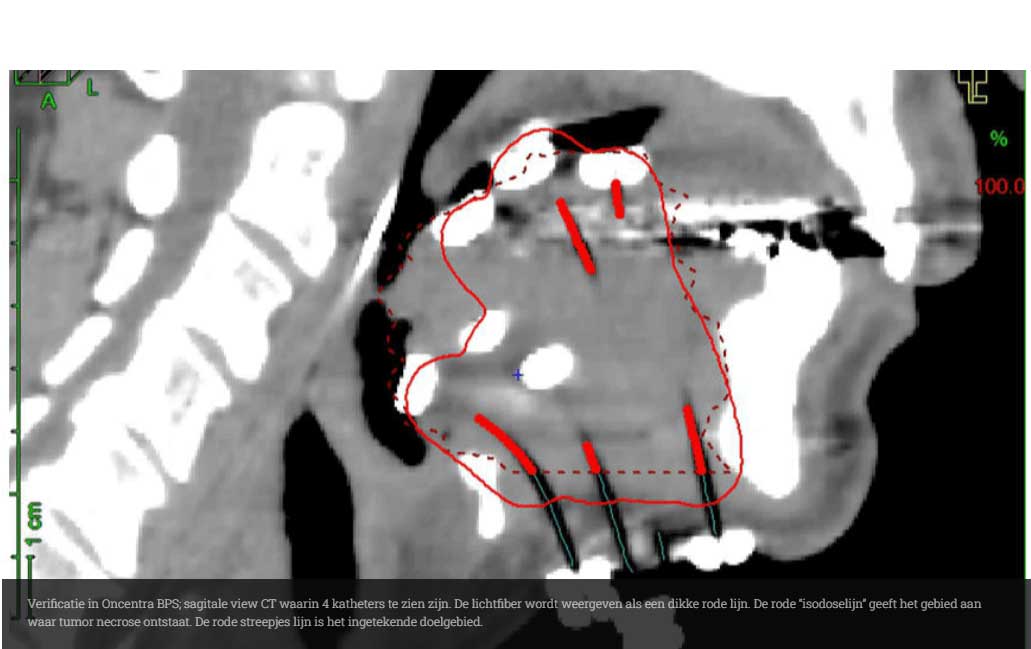
Verificatie middels CT
Op de OK worden de geplande katheters geïmplanteerd. Na de implantatie wordt er een verificatie CT gemaakt. Deze CT wordt vervolgens geregistreerd met de MRI waarop het doelgebied is ingetekend. In Oncentra BPS wordt deze registratie samen met de CT en ingetekende MRI geïmporteerd. Op de CT zijn de katheters goed zichtbaar en kunnen deze gereconstrueerd worden. Vervolgens wordt de belichting gesimuleerd door lichtbronnetjes in de katheters aan te zetten. Door het ingetekende doelgebied te projecteren op de CT, kan nu worden bepaald of het doelgebied goed wordt gecoverd door de geïmplanteerde katheters. Is dit niet het geval dan kan vooraf aan de belichting op de OK nog katheters worden bijgeplaatst. Als alle katheters geplaatst zijn volgt de belichting. Voor een uitvoerige beschrijving van deze procedure zie het artikel [1] in Lasers in Surgery and Medicine (2013).
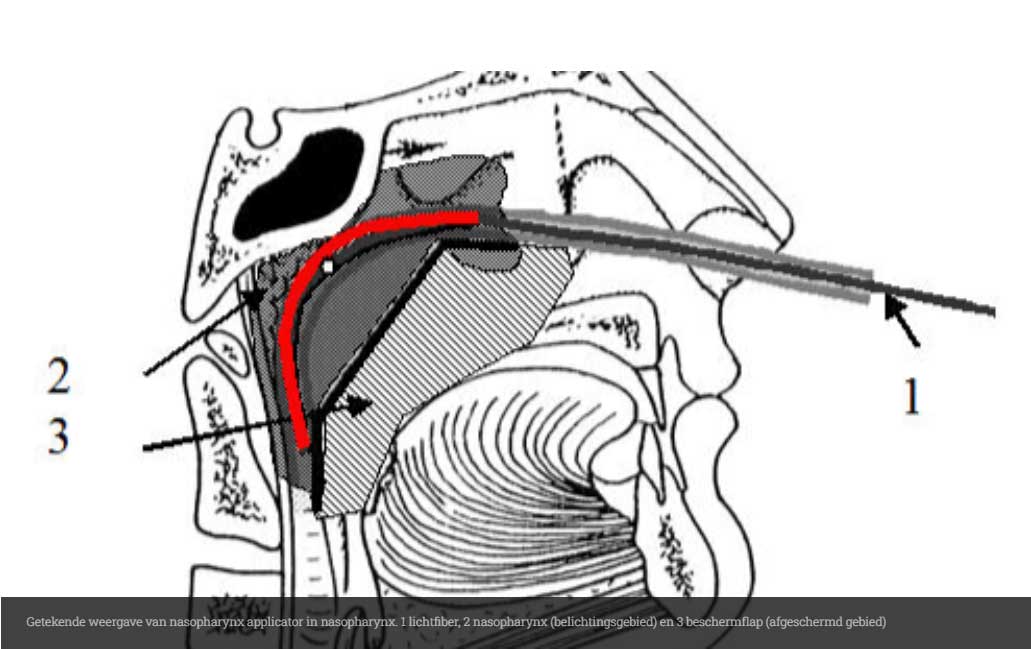
Intraluminaire belichting
Naast oppervlakkige en interstitiële belichting bestaat ook nog intraluminaire belichting. Dit wordt gedaan bij recidief nasopharynxcarcinoom. Voor de belichting wordt een nasopharynx applicator ingebracht, deze applicator is in Rotterdam ontwikkeld en lijkt veel op de “Rotterdam applicator” die voor brachytherapie wordt gebruikt. In deze applicator wordt weer een lichtfiber geplaatst, en op deze manier wordt de nasopharynx belicht.
Een van de ontwikkelingen waar we mee bezig zijn, is om te onderzoeken of PDT van de neus- en bijholten mogelijk is. De behandelopties bij een recidief en residu in deze bijholten zijn nu zeer beperkt. We hebben het afgelopen jaar een aantal patiënten behandeld met PDT en de resultaten zijn hoopgevend. Vanaf dit jaar gaan we samen met het ErasmusMC deze behandeling in studieverband verder optimaliseren.
Teamwork
De uitkomst van de PDT behandeling is, bij een goede indicatiestelling, vergelijkbaar aan de standaardtherapieën chirurgie en radiotherapie. PDT kan daarom gezien worden als een effectieve behandelmethode bij een lokale vorm van hoofd-halskanker naast chirurgie, radiotherapie en chemotherapie. Voor uitbehandelde patiënten kan het zelfs de enige optie zijn.
Om PDT behandelingen succesvol te kunnen uitvoeren is het belangrijk om een goed PDT team te hebben. Het PDT team uit het AvL bestaat uit:
- Hoofd-hals chirurgen
- Radiotherapeuten
- Verpleegkundig specialist
- PDT coördinator
- Fysici
Zo zorgen de hoofdhals chirurgen en radiotherapeuten, via een multi disciplinair overleg, voor een juiste indicatiestelling en wegen zij de mogelijk verschillende behandelopties af. De hoofdhals chirurg voert de PDT behandeling uit, voor interstitiële PDT gebeurt dit samen met een radiotherapeut. De verpleegkundig specialist zorgt voor een goede voor- en nazorg van de patiënt. Evenals de PDT coördinator die ook de logistiek regelt. De fysici bedienen de laser en zijn betrokken bij het bepalen van het belichtingsplan.
PDT wordt in het AvL niet alleen gebruikt voor hoofdhals tumoren, maar ook voor huidtumoren en recentelijk heeft de afdeling urologie meegedaan met een fase 3 studie voor PDT bij beginnend prostaatkanker [2].
Referenties
I.B. Tan et al, Fotodynamische therapie bij hoofd-halskanker, Nederlands tijdschrift voor oncologie, Vol. 6 Nr. 7, 2009.
[1] Baris Karakullukcu et al, MR and CT based treatment planning for mTHPC mediated interstitial photodynamic therapy of head and neck cancer: description of the method. Lasers in surgery and medicine 2013; 45:517-523.
[2] Abdel-Rahmene Azzouzi et al, Padeliporfin vascular-targeted photodynamic therapy versus active surveillance in men with low-risk prostate cancer (CLIN1001 PCM301): an open-label, phase 3, randomised controlled trail. Published online 2016 Dec; http://dx.doi.org/10.1016/S1470-2045(16)30661-1.