Extreem vroeggeboorte
Klinische relevantie
Jaarlijks worden wereldwijd 15 miljoen kinderen te vroeg geboren ( Naast korte termijn complicaties, zoals het Respiratoir Distress Syndroom (RDS), bronchopulmonale dysplasie (BPD), necrotische enterocolitis (NEC) en intraventriculaire bloeding (IVH), zijn er ook lange termijn complicaties, zoals neurocognitieve ontwikkelingsstoornissen [4].
PLS Technologie
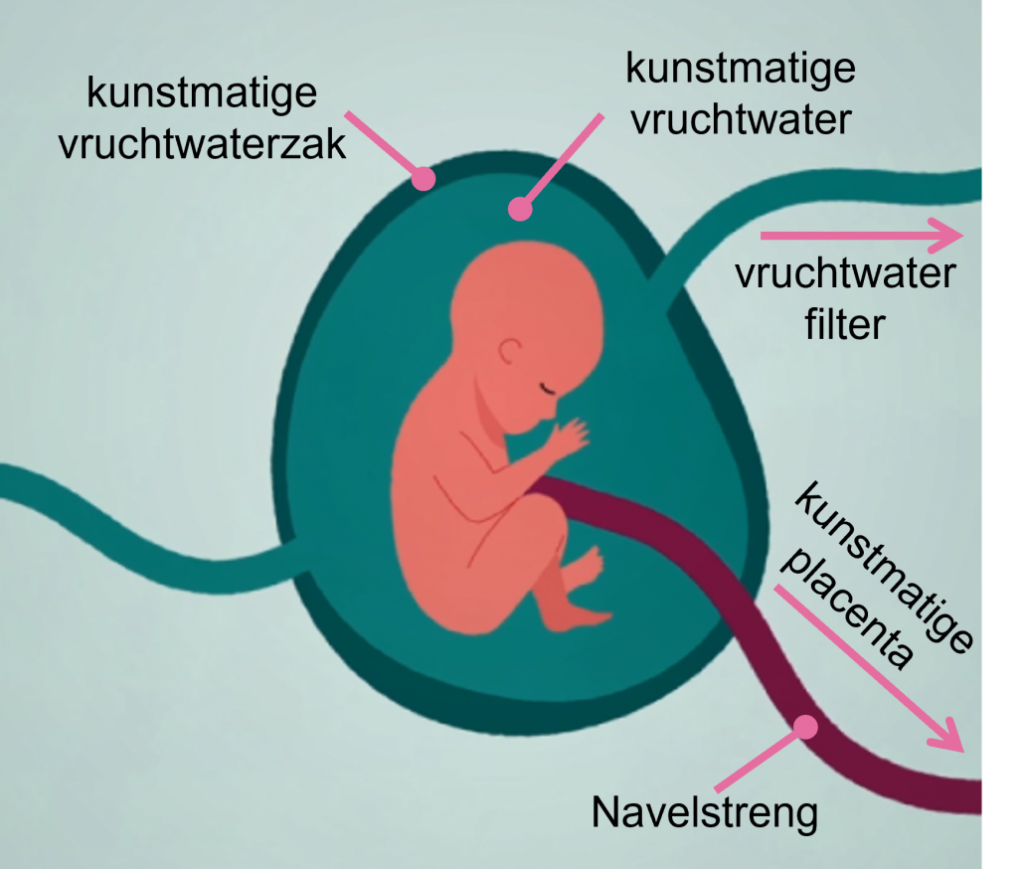
Om de levensverwachting en kwaliteit van deze groep te verbeteren, is er onderzoek gaande om een oplossing te creëren die de baarmoederomgeving beter nabootst dan de huidige couveuse. Op deze manier kunnen de organen van de extreem vroeg geboren baby’s verder groeien net zoals in de baarmoeder. Deze fundamenteel nieuwe visie op de couveuse, biedt een vloeistof-gevulde omgeving in combinatie met een kunstmatige placenta [3,7] (Figuur 1). De combinatie van de kunstmatige placenta en vruchtwaterzak faciliteert dat de organen verder kunnen rijpen terwijl de schadelijke effecten van mechanische beademing op de longen wordt voorkomen. Het doel van deze nieuwe technologie is om de overlevingskansen te vergroten, de kans op morbiditeit te verkleinen en de extreem vroeg geborenen door de kritieke periode van 24 tot 28 weken te helpen. In Europa is het multidisciplinaire Perinatal Life Support (PLS) consortium opgericht om een dergelijke couveuse, ofwel PLS-systeem te ontwikkelen. Het consortium heeft een grote variatie aan kennis en expertise: TU Eindhoven, RWTH Aachen, Politecnico di Milano, LifeTec Group, Nemo Healthcare, Medsim en Máxima Medisch Centrum.
Om het PLS-systeem – en het ecosysteem aan protocollen en andere tools – te ontwerpen en ontwikkelen is het noodzakelijk om de situatie zo realistisch mogelijk te testen. Preklinische diermodellen zijn gebruikt voor een proof-of-principle om deze nieuwe generatie van couveuses te testen bij foetale lammeren [2,3,7]. Desondanks is de stap van dierproeven met een volledig ontwikkeld PLS-systeem naar menselijke studies is nog steeds immens. Zowel dierproeven als humane klinische studies tijdens PLS-systeem ontwikkeling zijn moeilijk te realiseren vanwege de ethische bezwaren. Een groot deel van de aandacht in het ethische debat rond de ontwikkeling van het PLS-systeem is gevestigd op de implicaties op lange termijn, maar ook de ethische zorgen op korte termijn, zoals de inzet van dierstudies, moeten niet over het hoofd worden gezien [5].
Simulatie studies
Gezien we het uitvoeren van dierproeven ter ontwikkeling van de technologie zoveel mogelijk willen voorkomen, is validatie van de technische prototypes een grote uitdaging. Een veelbelovend alternatief voor het succesvol ontwikkelen van medische hulpmiddelen, het verbeteren van de kwaliteit van zorg en het faciliteren van trainingen zonder dierproeven, kan worden gevonden in het creëren van een medische simulatie. Deswege, ontwikkelen wij binnen dit project foetale manikins (Faculteit Industrial Design, TU Eindhoven) en digital twins (Faculteit Biomedical Engineering, TU Eindhoven) om de foetale patiënt zowel anatomisch als fysiologisch na te bootsen. Op deze manier kan het testen op proefdieren en valideren in mensen worden uitgesteld tot een stadium waarin de onderzoeksresultaten aanzienlijk minder onvoorspelbaar zijn.
Methode & resultaten
Manikin
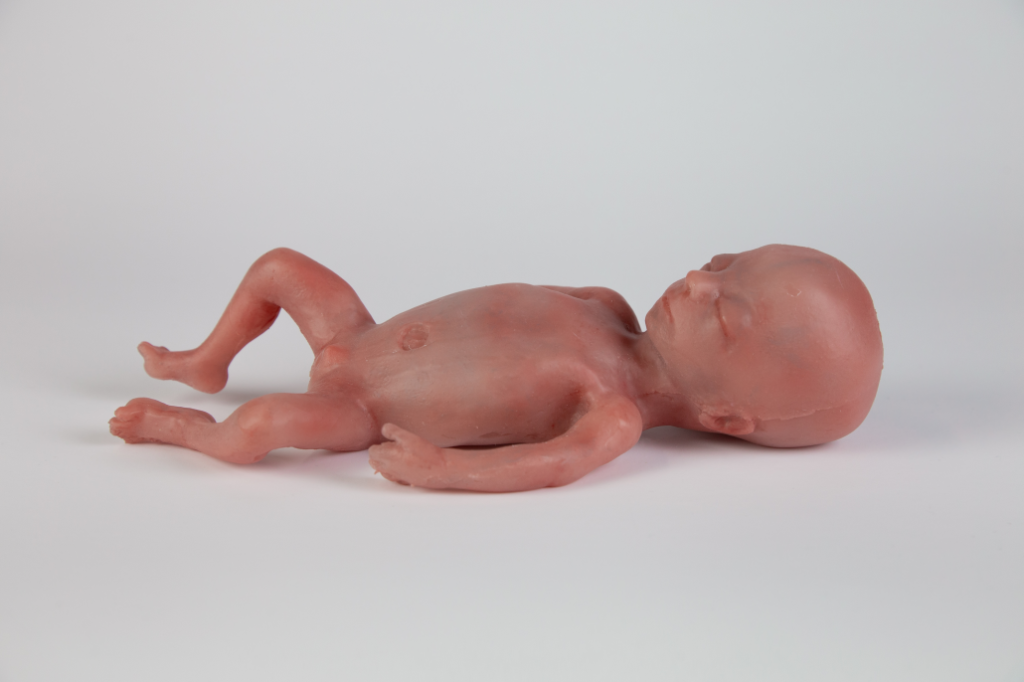
Om een realistisch fysiek 3D-model van een foetus te ontwikkelen, gebruikten we MRI-beelden van een foetus met een zwangerschapsduur van 24 weken als basis voor het ontwerp van de manikin. Door middel van 3D-printing technieken en gietmethodes kon deze worden gefabriceerd in siliconen. Literatuuronderzoek bracht de meest relevante fysiologische en fysieke componenten in kaart die een rol spelen bij gebruik van dit PLS-systeem. Op basis hiervan is een selectie aan sensoren en actuatoren (motors om symptomen te simuleren) geïntegreerd in de manikin. Denk aan onder andere temperatuurmonitoring, maar ook aan de simulatie van cyanose, hartslag, ademhaling en beweging. Het opnemen van foetale cardiorespiratoire fysiologie in de manikin met functies zoals een bloedstroom en hartslag kan ons informeren of er een aanhoudende circulatie tot stand is gebracht tussen het PLS-systeem en de foetus.
Digital twin
De digital twin in dit project is een virtuele representatie van de baby in het PLS-systeem die in contact staat met de echte baby in het PLS-systeem via metingen van de baby. De digital twin is een wiskundig model dat bestaat uit een gedetailleerd vaatstructuur, waar bloedstroming en -druk in elk vat berekend kan worden. Verder, kan het wiskundig model zuurstofdistributie, stofwisseling, foetale groei, baro- en chemoreceptor reflexen, en interactie tussen baby en de PLS componenten simuleren. Informatie voor, en verificatie van dit wiskundig model is gebaseerd op literatuur en retrospectieve klinische studies. Tijdens de ontwikkelingsfase van het PLS-systeem heeft de ‘digital twin’ als functie om meer informatie te vergaren over de interactie tussen baarmoeder en baby om zo de meest optimale omgeving te ontwikkelen. Als het PLS-systeem eenmaal in de kliniek wordt gebruikt dan kan de digital twin worden gebruikt als ondersteuning voor klinische besluitvorming door het effect van een apparaat instelling of interventie te voorspellen.

Interactie digital twin en manikin
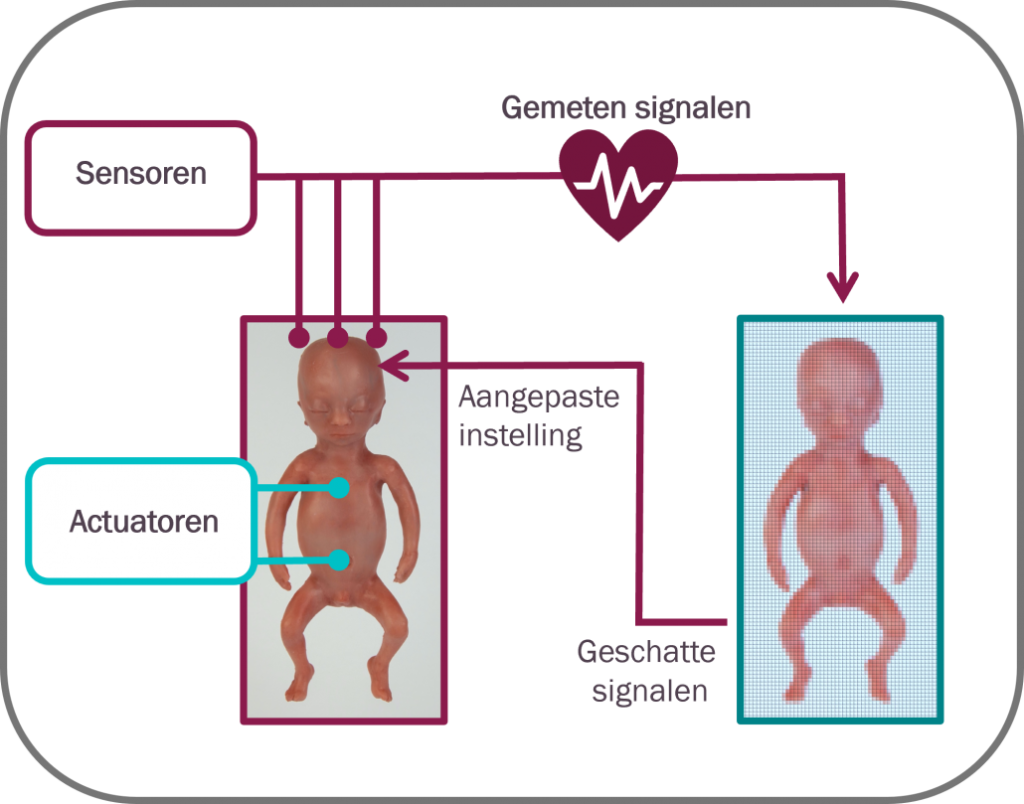
Door de digital twin met de manikin te verbinden, kan het effect van het PLS-systeem en de handelingen van het medisch personeel op de baby voorspeld worden. Op deze manier kan het systeem aangepast worden tot de meest optimale omgeving voor de baby. Daarnaast kunnen er levensechte situaties gesimuleerd worden om zorgprofessionals te trainen. Figuur 4 beschrijft een voorbeeld van een mogelijke interactie tussen een manikin en digital twin. De manikin bevat actuatoren die levensechte signalen van de zuurstofsaturatie in de hersenen, hartslag en bloedstroming in de navelstreng kan generen. Deze signalen worden gelezen door sensoren en worden gebruikt door de digital twin. Vervolgens wordt de perifere zuurstofsaturatie geschat. De geschatte en gemeten signalen worden gebruikt om een voorspelling te doen over het welzijn van de baby. Bij verslechtering van de conditie van de (gesimuleerde) baby kunnen relevante symptomen gesimuleerd worden door de manikin. Op deze manier kan het zorgpersoneel adequaat reageren tijdens een training of door instellingen van het PLS-systeem te optimaliseren om zo een ideale omgeving te creëren voor de baby.
Discussie
Het doel van de simulatie is drieledig; het kan ten eerste dienen als methode om prototypes en medische protocollen van het PLS-systeem in een vroeg stadium te optimaliseren en valideren. Ten tweede, het functionele prototype kan getest worden met (nieuwe) klinische protocollen, zodat het kan worden gebruikt als middel om medisch personeel te trainen met deze nieuwe technologie in een veilige setting. Het gebruik van het PLS-systeem omvat complexe taken die precisie, teamwerk en correct tijdsmanagement vereisen. Door het gebruik van een simulatie kunnen klinische scenario’s volledig gecontroleerd worden, waardoor noch de (gesimuleerde) patiënt, noch het zorgteam in een (psychologisch of fysiek) onveilige situatie gebracht worden. Daarnaast heeft de gesimuleerde omgeving veel vrijheidsgraden. Er kunnen verschillende scenario’s worden nagebootst met een lage incidentie, maar met een hoog risico. Binnen een medische training komt deze vrijheid van pas, omdat men in een korte tijd zeer vertrouwd kan raken met complexe procedures en de bijbehorende hulpmiddelen. Afwijkingen, patiënten met specifieke complicaties of zelfs verschillende medische teamsamenstellingen kunnen op deze manier moeiteloos en veelvuldig worden gesimuleerd. Ten derde, wanneer het PLS-systeem is geïmplementeerd in de kliniek, kunnen de simulaties ondersteuning bieden aan klinische besluitvorming. Signalen die gemeten worden bij de baby kunnen worden gebruikt voor een patiënt-specifieke simulatie. Deze simulatie kan dan signalen schatten die niet gemeten kunnen worden. Gebaseerd op de geschatte en gemeten signalen kan er een advies gegeven worden aan de arts over PLS-systeeminstellingen en, indien nodig, mogelijke interventies.
Future outlook
Hoewel de definitieve validatie van het PLS-systeem ook dierproeven zal moeten omvatten, stellen we een simulatie-gebaseerde validatie voor, door de fysieke manikin te combineren met een digital twin. Het gebruik van simulatietechnologie om een ‘life-support’ systeem te valideren is ongekend in de neonatologie. Een proof-of-concept prototype wordt over ongeveer 2 jaar verwacht, als het Horizon 2020 PLS project ten einde loopt.
Referenties
[1] Glass, H. C., Costarino, A. T., Stayer, S. A., Brett, C. M., Cladis, F., & Davis, P. J. Outcomes for extremely premature infants. Anesthesia and analgesia (2015). 120(6), 1337–1351.
[2] Hornick, M. A., Davey, M. G., Partridge, E. A., Mejaddam, A. Y., McGovern, P. E., Olive, A. M., … Flake, A. W. Umbilical cannulation optimizes circuit flows in premature lambs supported by the EXTra-uterine Environment for Neonatal Development (EXTEND). The Journal of Physiology (2018). 596(9), 1575–1585.doi:10.1113/jp275367
[3] Partridge, E. A., Davey, M. G., Hornick, M. A., McGovern, P. E., Mejaddam, A. Y., Vrecenak J. D… Flake, A. W. An extra-uterine system to physiologically support the extreme premature lamb. Nature Communications. (2017). 8, 1–15;
[4] Patel R. M. Short- and Long-Term Outcomes for Extremely Preterm Infants. American journal of perinatology. (2016). 33(3), 318–328.
[5] Romanis EC. Artificial womb technology and clinical translation: Innovative treatment or medical research? Bioethics. (2019). 00:1–11.
[6] Torchin, H., & Ancel, P.-Y. Épidémiologie et facteurs de risque de la prématurité. Journal de Gynécologie Obstétrique et Biologie de la Reproduction. (2016). 45(10), 1213–1230.
[7] Usuda, H., Watanabe, S., Saito, M., Sato, S., Musk, G. C., Fee, M. E., Kemp, M. W. Successful use of an artificial placenta to support extremely preterm ovine fetuses at the border of viability. American Journal of Obstetrics and Gynecology. (2019). 221(1).







