Trauma aan het aangezicht kan ontstaan door verschillende oorzaken, zoals verkeersongevallen, een val, sportincidenten of geweld. Naast levensbedreigende klachten kan het optreden van aangezichtstrauma leiden tot verlies van vorm (bijvoorbeeld verlies van projectie van het jukbeen) en functie (bijvoorbeeld visusstoornissen na een factuur van de oogkas). Bij de behandeling wordt gepoogd het vorm- en functieverlies zo goed mogelijk te herstellen. Het is van belang om minimaal invasief te werken vanuit ‘verborgen’ benaderingen zoals intraoraal, transconjunctivaal of coronaal, om het aanbrengen van zichtbare littekens in het aangezicht door de chirurgie te voorkomen. Technologische hulpmiddelen kunnen de chirurg hierbij helpen te oriënteren op de complexe anatomie en overzicht te genereren in moeilijk bereikbare of weinig overzichtelijke delen van het aangezicht.1
Het gebruik van deze technologische hulpmiddelen zit ingesloten in het principe van computer-geassisteerde chirurgie. Toch is computer-geassisteerde chirurgie meer dan alleen de inzet van technologie tijdens de operatie: er kunnen ook een preoperatieve planningfase en postoperatieve evaluatiefase worden onderscheiden. Een overzicht van computer-geassisteerde chirurgie bij aangezichtstrauma en enkele voorbeelden zullen hieronder worden gegeven. Het ultieme doel van computer-geassisteerde chirurgie is het behalen van het optimale operatieresultaat (en hiermee klinische einduitkomst) door het vergroten van de nauwkeurigheid en efficiëntie van de operatie.
De virtuele planning
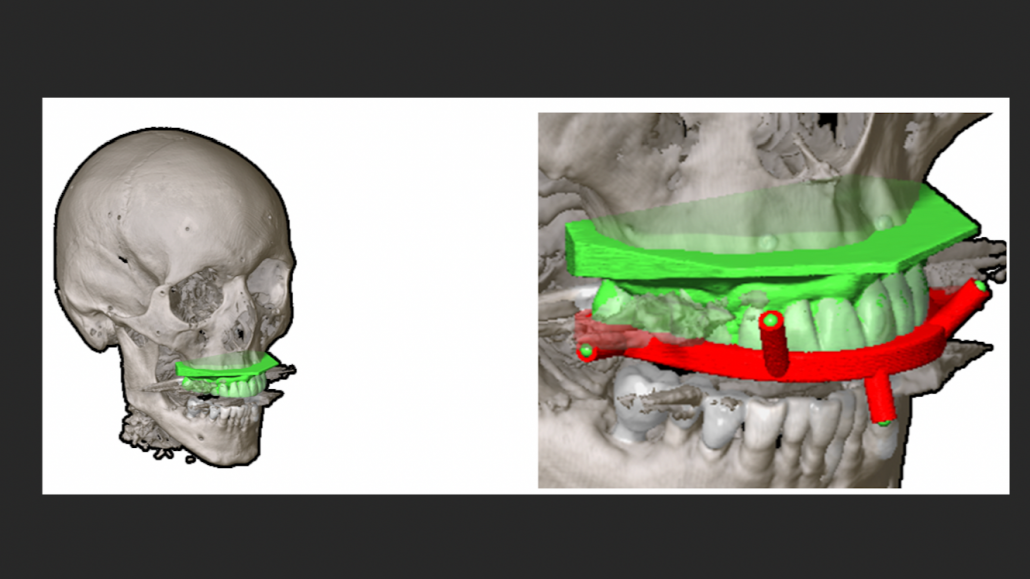
In de preoperatieve fase van computer-geassisteerde chirurgie wordt dit optimale resultaat gesimuleerd op basis van de beeldvorming. Binnen de aangezichtstraumatologie wordt hierbij vaak gebruik gemaakt van een computer tomography (CT) scan. Een CT-scan is een virtuele weergave van de patiënt die bestaat uit verschillende volume-elementjes, voxels, met een grijswaarde (Hounsfield Unit) die correspondeert met de absorptie van de Röntgenstraling binnen die voxel. Vanuit de CT-scan kunnen coupes in verschillende richtingen worden gereconstrueerd, maar bij computer-geassisteerde chirurgie is het juist het idee om verder te gaan dan bekijken van de beelden alleen: informatie wordt geëxtraheerd en toegevoegd aan de beeldvorming om zo tot een uitgebreidere analyse te komen: de geavanceerde diagnostiek. Veelal wordt hierbij gebruik gemaakt van gespecialiseerde software, specifiek voor aangezichtsanalyse. Het is hierbij zelfs mogelijk om andere beeldvormingsmodaliteiten to fuseren met de CT-scan, bijvoorbeeld een intraorale scan van de dentitie, om een zo volledig mogelijke virtuele weergave van de patiënt te krijgen (Figuur 1).
Segmentatie kan worden gezien als het werkpaard van de geavanceerde diagnostiek. De scan wordt opgedeeld in voxels die tot dezelfde anatomische structuur behoren. Een voorbeeld van een segmentatiemethode is thresholding, waarbij een grijswaarde als afkapwaarde wordt gekozen om de voxels te selecteren. Hiermee kunnen bijvoorbeeld de benige delen geselecteerd worden, terwijl de weke delen niet worden aangeduid. Meer geavanceerde segmentatiemethoden maken het mogelijk segmentaties van individuele botstructuren, zoals de oogkas of het jukbeen, te genereren. Hiermee kunnen ook hiaten in de thresholdingoperatie (zoals het niet includeren van de dunne botwanden van de oogkassen) worden opgevuld. De segmentatie kan worden gevisualiseerd als een kleurenoverlay in de coupes, maar biedt ook verdergaande mogelijkheden. Er kan een 3D weergave van de segmentatie worden gegenereerd (zoals van de botstructuren in Figuur 1) en de gesegmenteerde structuren kunnen worden gemanipuleerd.
Het spiegelen van gesegmenteerde botstructuren is een manipulatiemethode die veel wordt toegepast binnen de aangezichtstraumatologie. Bij enkelzijdig trauma, zoals een oogkasfractuur of een jukbeenfractuur, wordt een segmentatie van de onaangedane zijde gegenereerd en vervolgens gespiegeld. Deze spiegeling wordt als een overlay weergegeven op de aangedane zijde en geeft een goede indicatie van de pretraumateuze anatomie. Een vergelijk tussen aangedaan en onaangedaan is heirmee veel gemakkelijker te doen dan visueel vergelijken van beide zijden in één van de coupes. De precieze grootte van het aangedane gebied en de verplaatsing van de botstructuren worden inzichtelijk gemaakt; het is zelfs mogelijk metingen uit te voeren om bijvoorbeeld de verplaatsing te kwantificeren. Voor het jukbeen dient de spiegeling ook direct als de virtuele chirurgische planning: het simuleert het gewenste chirurgische eindresultaat. Voor het voorbeeld van de oogkasreconstructie wordt een virtuele weergave van een voorgevormd implantaat zo gepositioneerd in de virtuele patiënt dat het de contour van de onaangedane, gespiegelde oogkas zo goed mogelijk volgt, met inachtneming van de positie van bestaande botstructuren, afsteuning en fixatiemogelijkheden. Het is zelfs mogelijk een implantaat volledig op maat te ontwerpen voor de patiënt (een patiënt-specifiek implantaat), om tot een optimale reconstructie te kunnen komen.
Bij omvangrijker, dubbelzijdig trauma wordt de spiegeling gebruikt om een zo compleet mogelijk beeld te krijgen; informatie over de pretraumateuze anatomie kan worden verkregen door het manipuleren van de positie van individuele botstukken (virtueel puzzelen) of het importeren van een referentie. Deze referentie kan van een andere patiënt met vergelijkbare anatomie zijn, maar uiteraard is er geen betere referentie dan de patiënt zelf! Een mooi praktijkvoorbeeld van dat laatste werd toegepast bij een secundaire reconstructie van een panfaciaal trauma, waarbij de bovenkaak en onderkaak breed rereconstrueerd waren. De orthodontist beschikte over gebitsmodellen van voor het ongeval, de digitale tandmodellen voegde een perfecte referentie toe voor de gewenste breedte. De breedte van de onderkaak en bovenkaak in de virtuele patiënt konden hierna worden aangepast op basis van deze informatie (Figuur 3).
Dit laatste voorbeeld benadrukt dat het belangrijk is altijd alle informatie te verzamelen en te gebruiken in de preoperatieve fase. Daarnaast zijn ook gespecialiseerde software, kennis van gebruikte beeldvormingstechnieken en technologische mogelijkheden en natuurlijk klinische kennis en ervaring van groot belang. Voor aangezichtstraumatologie en breder voor meerdere operaties binnen het specialisme Mondziekten, Kaak- en Aangezichtschirurgie worden deze preoperatieve voorbereiding daarom gedaan door een technisch geneeskundige in nauw overleg met de behandelend chirurg. Het is mogelijk verschillende scenario’s te simuleren in de virtuele planning en zo tot een zo optimaal mogelijke planning te komen. Tijdens de operatieve fase van computer-geassisteerde chirurgie geeft de planning het gewenste chirurgische resultaat waar naartoe wordt gewerkt. Een deel van de puzzel is al vooraf gedaan. Het is echter ook mogelijk verdergaande feedback op de virtuele planning te verkrijgen in de operatieve fase van computer-geassisteerde chirurgie, door middel van chirurgische guidance.
Chirurgische guidance
Chirurgische guidance zorgt voor een overdracht van de preoperatieve planning naar de chirurgische setting. De chirurg kan door middel van chirurgische guidance feedback ontvangen tijdens de chirurgie en actief naar het gewenste resultaat worden geleid. Hierbij kunnen grofweg drie verschillende methoden worden onderscheiden: statische guidance, dynamische guidance en image guidance. Statische guidance richt zich op het geven van feedback op één positie (bij één handeling) en is gecentreerd rond het 3D printen van hulpstukken voor de operatie. Een voorbeeld van indirect gebruik is het 3D printen van een virtueel planmodel, waarop osteosynthesemateriaal kan worden voorgebogen. Bij het plaatsen van het osteosynthesemateriaal geeft de vorm feedback over de gewenste positie van de botdelen waarop het gefixeerd moet worden. Naast deze indirecte vorm kunnen 3D geprinte hulpstukken ook direct in het lichaam feedback geven, zoals boor- en zaagmallen om boor- en zaagposities te controleren. In het voorbeeld van Figuur 3 werd een dentale splint geprint, waarin de geplande tandposities van boven- en onderkaak vastliggen, wat dient als een soort positioneringsmal. Wanneer er bij een secundaire ingreep al boorposities beschikbaar zijn van eerder geplaatst osteosynthesemateriaal, kunnen deze worden ingebed in het ontwerp van een patiënt-specifieke implantaat om zo te zorgen dat het implantaat ook op de gewenste positie wordt ingebracht.
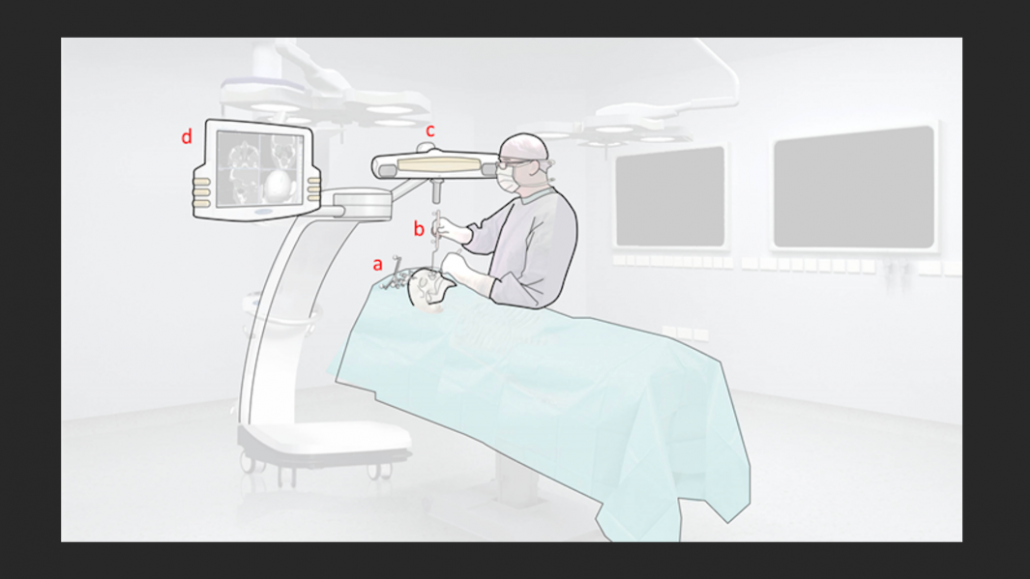
Chirurgische navigatie kan tijdens de ingreep dynamische feedback voorzien. De positie van een navigatiepointer en de positie van de patiënt worden tijdens de ingreep in de operatieruimte gevolgd (tracking) door een camera (Figuur 4). Hier kunnen onder andere optische markers voor worden gebruikt: lichtreflecterende bolletjes op het instrument en gefixeerd op de patiënt, in een standaard geometrie. De navigatiecamera volgt de bolletjes in de ruimte; het systeem herkent de onderliggende geometrie en weet dus welke bolletjes bij patiënt en instrument horen. Feedback op de planning wordt gegeven door de fysieke positie van de pointer virtueel in de planning te visualiseren. Om dit de bewerkstelligen, moet eerst de patiënt gekoppeld worden aan de virtuele planning: de registratie. Deze koppeling dient nauwkeurig te gebeuren omdat er anders een discrepantie tussen eigenlijke situatie en feedback ontstaat (registratiefout). Er zijn velerlei methoden voor registratie van patiënt en scan, zoals oppervlakteregistratie van weke delen (door zwelling vaak onbruikbaar bij trauma) of puntsgewijze registratie op schroeven die zichtbaar zijn op de scan. Door de genoemde fusie van de gebitsmodellen is het tegenwoordig echter ook mogelijk een registratiesplint te gebruiken, wat een non-invasieve methode is die ook nog de (veelal) additionele CT-scan met de geplaatste schroeven weet te voorkomen.
Na registratie kan de positie en beweging van de pointer in de patiënt worden vergeleken met de planning. Zo kan bijvoorbeeld de gereconstrueerde buitencontour van het bot worden vergeleken. Bij het plaatsen van een oogkasimplantaat kan de pointer op fysieke herkenningspunten op het implantaat worden gepositioneerd, waarbij visuele én kwantitatieve feedback wordt verkregen ten opzichte van de geplande positie van dit markerpunt. Aan de hand van de feedback kan de reconstructie worden aangepast, waarna nogmaals kan worden gecontroleerd. In onderzoek naar verbetering van dit feedbackmechanisme voor het oogkasimplantaat is inmiddels ook workflow met real-time feedback ontwikkeld en ex-vivo gevalideerd, waarbij de positie van het implantaat tijdens het inbrengen wordt getracked in plaats van alleen achteraf gemeten.4
Intraoperatieve beeldvorming valt onder de laatste guidance categorie. De validatie en documentatie van het chirurgisch resultaat, die traditioneel postoperatief plaatsvond, kan met intraoperatieve beeldvorming nog tijdens de operatie worden gedaan. Deze intraoperatieve beeldvorming geeft een objectief en compleet overzicht van het bereikte resultaat. De intraoperatieve beeldvorming kan worden gefuseerd met de virtuele planning om een één-op-één vergelijk tussen beiden te kunnen maken. Wanneer de reconstructie toch afwijkend blijkt te zijn, kan in dezelfde chirurgische setting nog worden ingegrepen. Hiermee wordt de patiënt een vervolgoperatie bespaard gebleven.5,6
Al deze technologie op de operatiekamer is het stadium van gadget al lang voorbij. In verschillende onderzoeken is de effectiviteit van computer-geassisteerde chirurgie aangetoond.7–9 Naast de virtuele planning is er ook een rol voor de technisch geneeskundige weggelegd in de intraoperatieve fase, voornamelijk wanneer de inzet van nieuwe technologie of een complexe operatieplanning betreft. De samenwerking tussen chirurg en techneut op de OK zal dan zorg dragen voor het correct gebruik van de verschillende technologiën of hulpstukken én de juiste interpretatie van de feedback. De ervaring tijdens de chirurgie kan daarnaast aanleiding vormen tot het maken van verbeterstappen in de inzet van technologie (bijvoorbeeld de splintregistratie of real-time navigatie) of aanpassingen in de virtuele planning van volgende patiënten.
Postoperatieve evaluatie
In de postoperatieve fase wordt het chirurgisch resultaat geëvalueerd (Figuur 6). De beeldfusie van intraoperatieve of postoperatieve beeldvorming met de chirurgische planning is hierin vaak de eerste stap. Verschillende kwantificatiemethoden kunnen worden ingezet om het resultaat te objectiveren; de laatste jaren richten veel van deze methoden zich op automatische 3D analyse van het resultaat.10 Er dient kritisch te worden geëvalueerd om te oordelen of het behaalde resultaat binnen de foutmarge ligt en waar mogelijke verbeterpunten (in de hele workflow) zitten. Wanneer de evaluatie aanleiding geeft tot een verandering in het proces, bijvoorbeeld de inzet van een nieuwe techniek, kan ook het effect objectief worden gemeten door de kwantitatieve resultaten met en zonder verandering te vergelijken. Hiermee wordt de computer-geassisteerde chirurgie als geheel zo optimaal mogelijk ingericht en kan de patiënt zo accuraat en efficiënt mogelijk worden behandeld.

Dit artikel is geschreven door Ruud Schreurs, onderzoeker bij afdeling MKA Amsterdam UMC en MKA Radboudumc.
Afbeeldingen © Ruud Schreurs
Referenties
- Dubois L., Schreurs R., Lapid O., Saeed P., Adriaensen GF., de Jong VM. Multidisciplinaire aanpak bij aangezichtsletsel. Ned Tijdschr Geneeskd 2017;161(D1537).
- Schreurs R., Klop C., Maal TJJ. Advanced Diagnostics and Three-dimensional Virtual Surgical Planning in Orbital Reconstruction. Atlas Oral Maxillofac Surg Clin North Am 2021;29(1):79–96.
- Schreurs R., Baan F., Klop C., Dubois L., Beenen LFM., Habets PEMH., et al. Virtual splint registration for electromagnetic and optical navigation in orbital and craniofacial surgery. Sci Rep 2021;11(1):1–12. Doi: 10.1038/s41598-021-89897-8.
- Schreurs R., Dubois L., Ho J., Klop C., Beenen LFM., Habets P., et al. Implant-oriented navigation in orbital reconstruction part II: preclinical cadaver study. Int J Oral Maxillofac Surg 2020;49(5):678–85.
- Schreurs R., Wilde F., Schramm A., Gellrich N-C. Intraoperative Feedback and Quality Control in Orbital Reconstruction: The Past, the Present, and the Future. Atlas Oral Maxillofac Surg Clin North Am 2021;29(1):97–108.
- Jansen J., Schreurs R., Dubois L., Maal TJJ., Gooris PJJ., Becking AG. Intraoperative imaging in orbital reconstruction: how does it affect the position of the implant? Br J Oral Maxillofac Surg 2020;58(7):801–6.
- Yu H., Shen SG., Wang X., Zhang L., Zhang S. The indication and application of computer-assisted navigation in oral and maxillofacial surgery—Shanghai’s experience based on 104 cases. J Cranio-Maxillofacial Surg 2013;41(8):770–4.
- Zimmerer RM., Ellis E., Aniceto GS., Schramm A., Wagner MEH., Grant MP., et al. A prospective multicenter study to compare the precision of posttraumatic internal orbital reconstruction with standard preformed and individualized orbital implants. J Cranio-Maxillofacial Surg 2016;44(9):1485–97.
- Schreurs R., Becking AG., Jansen J., Dubois L. Advanced Concepts of Orbital Reconstruction: A Unique Attempt to Scientifically Evaluate Individual Techniques in Reconstruction of Large Orbital Defects. Atlas Oral Maxillofac Surg Clin North Am 2021;29(1):151–62.
- Baan F., Sabelis JF., Schreurs R., van de Steeg G., Xi T., van Riet TCT., et al. Validation of the OrthoGnathicAnalyser 2.0—3D accuracy assessment tool for bimaxillary surgery and genioplasty. PLoS One 2021;16(1):e0246196.