Vanwege de bewezen diagnostische waarde voor veel klinische toepassingen gaat vaak de voorkeur uit naar Magnetic Resonance Imaging (MRI) als beeldvormende modaliteit om zacht weefsel van patiënten te onderzoeken. Een toenemend aantal patiënten is behandeld met metalen implantaten en er is een behoefte om zacht weefsel in de buurt van deze metalen implantaten te evalueren, vaak vanwege complicaties veroorzaakt door het implantaat of de chirurgische ingreep.
Contra-indicatie?
Chirurgen en radiologen geven aan dat voor veel ziektes het weefsel tot op een halve centimeter van het implantaat geëvalueerd moet kunnen worden. Voor een aantal metalen implantaten is een MRI onderzoek onveilig en dus gecontra-indiceerd. Voor andere implantaten kan het voor de patiënt veilig zijn om een MR onderzoek te ondergaan, mits alle veiligheidsvoorwaarden in acht worden genomen. Zelfs al is het veilig, metalen implantaten beïnvloeden het magnetische veld, veroorzaken „artefacten” (kenmerken in het beeld die niet met de werkelijkheid overeenkomen) en verminderen daarmee de beeldkwaliteit, hetgeen diagnose met behulp van deze beelden bemoeilijkt en soms zelfs onmogelijk maakt.
Het doel van het beschreven onderzoek en bijbehorend proefontwerp was om de artefacten in het beeld te reduceren en de beeldkwaliteit te herstellen opdat een correcte diagnose mogelijk wordt. Lees indien nodig eerst het artikel hoe werkt diagnostiek met magnetische resonantie. Vervolgens worden de technieken beschreven om metaalartefacten te reduceren. Hiertoe behoren zowel recent ontwikkelde bestaande technieken als ook de nieuwe technieken die voor het eerst zijn gebruikt in dit onderzoek.
Beeldartefacten door metalen implantaten
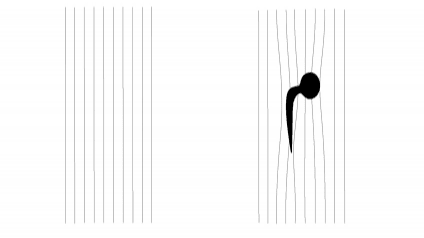
Vooral frequentiecodering en de selectie van het weefsel, dat als gevolg van de RF-puls een signaal geeft, zijn sterk afhankelijk van de Larmor frequentie. Voor een betrouwbare Larmor frequentie van alle kernen in de MRI scanner is het essentieel dat het magnetische veld in de gehele tunnel extreem homogeen is. Wanneer echter een patiënt met een metalen implantaat de MRI-scanner in gaat, wordt het magnetische veld lokaal afgebogen door het implantaat (Figuur 1), waardoor de veldhomogeniteit significant verslechtert.
De resulterende ruimtelijke variatie van het magnetische veld veroorzaakt aanzienlijke afwijkingen in de precessiefrequentie van de kernen. Aangezien deze frequentie wordt gebruikt voor het lokaliseren van het signaal, leiden de frequentieafwijkingen tot misplaatsing van het signaal in het beeld, met name in de frequentiecoderingsrichting. Bij 2D beeldvorming leiden de door het metaal geïnduceerde frequentieafwijkingen bovendien tot vervorming van het plakselectieprofiel dat anders recht zou zijn. Deze vervormingen veroorzaken op hun beurt weer andere artefacten in het beeld, waaronder lichte en donkere vlekken. Fasecodering daarentegen is ongevoelig voor veldsterkte variaties en dus ruimtelijk nauwkeurig zelfs in de buurt van metaal.
Bestaande technieken om metaalartefacten te reduceren
Hoewel er een aantal algemeen beschikbare technieken kunnen worden gebruikt om metaalartefacten binnen de perken te houden, blijven er altijd artefacten over. Deze artefacten zijn vaak te groot om evaluatie van weefsel mogelijk te maken op een halve centimeter afstand van het implantaat. Daarom zijn er in de afgelopen jaren meer geavanceerde technieken ontwikkeld om metaalartefacten aan te pakken. Hiertoe behoren de multi-spectrale afbeeldingstechnieken (Multi-Spectral Imaging, MSI). MSI technieken reduceren metaalartefacten aanzienlijk, maar ten koste van een langere scantijd.
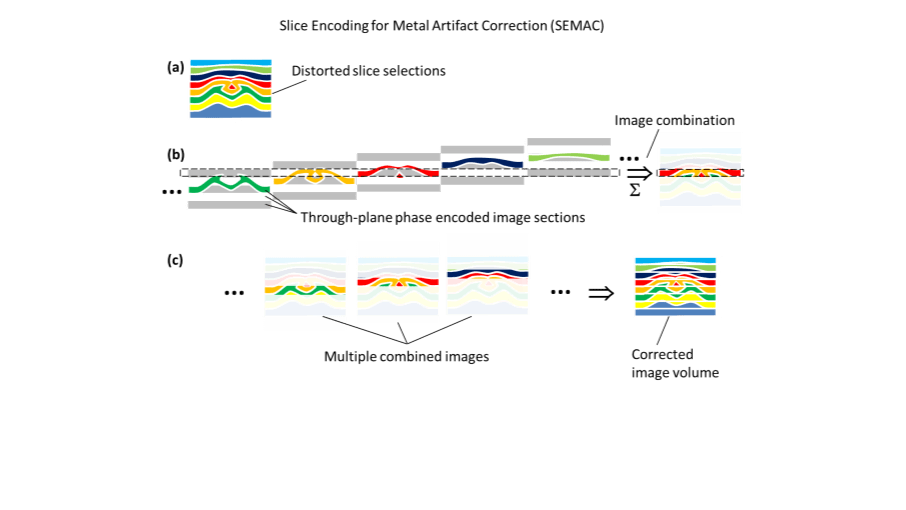
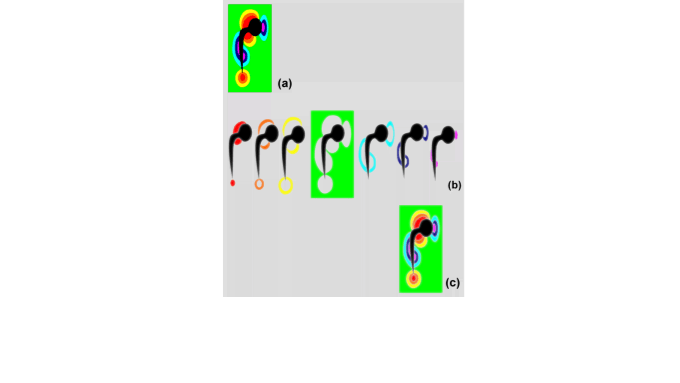
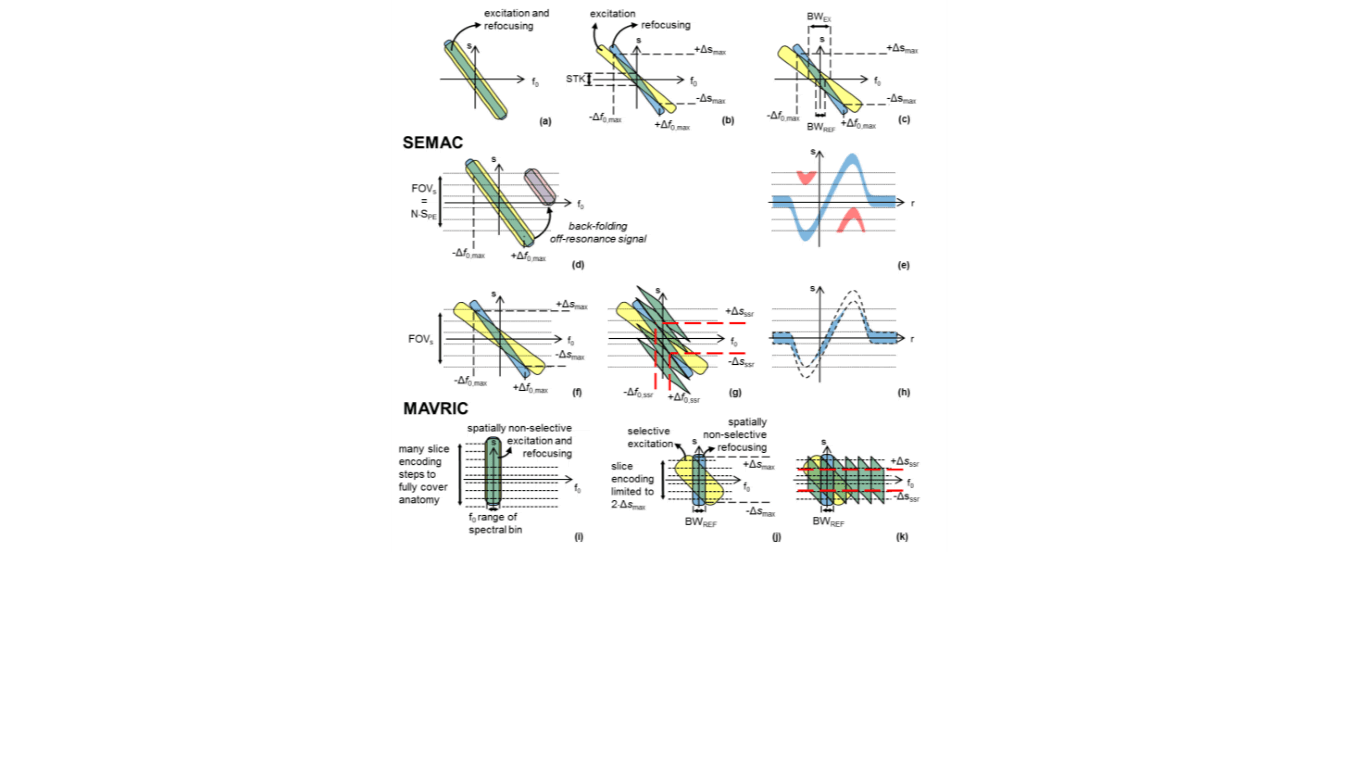
Voorbeelden van MSI technieken zijn SEMAC (Slice-Encoding for Metal Artifact Correction) en MAVRIC (Multi-Acquisition with Variable-Resonance Image Combination). SEMAC is gebaseerd op een multi-slice signaal acquisitie en lost plakvervorming op met een aantal extra fasecoderingsstappen in de richting loodrecht op het beeldvlak (Figuur 2). MAVRIC is gebaseerd op een 3D acquisitie met een beperkte frequentie-inhoud, en herhaalt deze acquisitie voor een aantal aangrenzende frequentiebanden, zogenaamde „spectral bins”, om het volledige frequentiespectrum af te dekken (Figuur 3). In beide MSI technieken wordt dus een conventionele acquisitie techniek meerdere malen herhaald om voldoende informatie te verzamelen over de locatie en de frequentie van MR signalen, met als gevolg een langere scantijd.
Het aantal fasecoderingsstappen in de richting loodrecht op het beeldvlak in MSI technieken is afhankelijk van het materiaal en de afmeting van het implantaat en het ruimtelijke gevoeligheidsprofiel van de ontvangstspoel. Te veel fasecoderingsstappen leiden tot overmatige toename van scantijd, maar te weinig fasecoderingsstappen dekken het MR-signaal niet volledig af, waardoor het MR-signaal zichtbaar wordt op een verkeerde positie in het beeld, of zelfs in het verkeerde beeld.
Innovaties in MSI
In het proefschrift wordt een nieuwe aanpassing van MSI technieken besproken, genaamd Off-Resonance Suppression (ORS, figuur 4). In de oorspronkelijke MSI technieken zijn de excitatiepuls en de daarop volgende refocuseringspulsen uitgelijnd en beïnvloeden beide soorten pulsen dezelfde waterstofkernen. Bij ORS daarentegen verschillen de twee soorten pulsen en overlappen ze slechts gedeeltelijk. Daardoor zijn er slechts een beperkt aantal kernen die zowel de excitatiepuls als de refocuseringspulsen ondervinden en die bijdragen aan het MR-signaal. Kernen met sterke frequentieafwijkingen op grote afstand van het beoogde afbeeldingsgebied ervaren slechts een van beide soorten pulsen en dragen niet bij aan het MR-signaal.
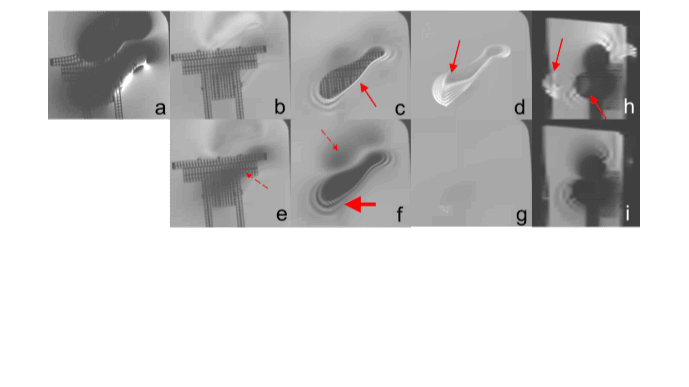
Deze wijziging van het selectieproces maakt een regelbare inperking van het MR-signaal mogelijk, en dus van het vereiste aantal fasecoderingsstappen om het MR-signaal volledig af te dekken. ORS maakt het dus mogelijk om de scantijd en de omvang van het MR-signaal tegen elkaar uit te ruilen zonder het risico op aliasing artefacten. ORS kan worden toegepast of verschillende MSI technieken waaronder SEMAC (ORS-SEMAC) en MAVRIC (ORS-MAVRIC). Voorbeelden hiervan zijn gedemonstreerd in fantoom- en vrijwilliger-experimenten (Figuur 5 t/m 8).
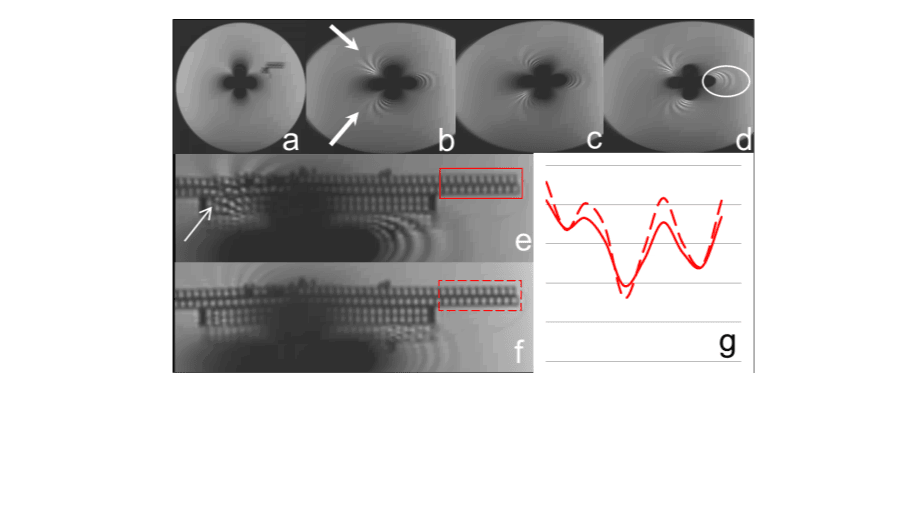
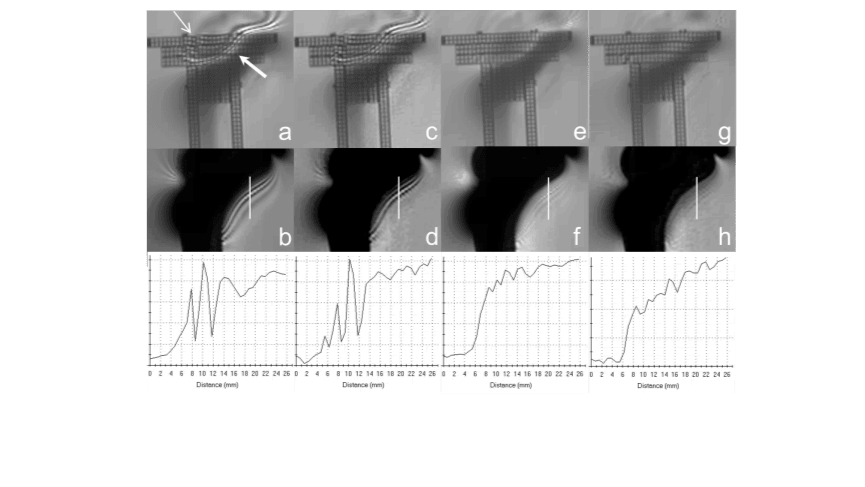
Een SEMAC-beeld kan signaal van meerdere plakselecties bevatten. Daardoor kan in SEMAC-beelden een resterend artefact voorkomen wanneer overgangen tussen naburige plakselecties zichtbaar worden, hetgeen resulteert in intensiteitsfluctuaties, aangeduid als het ripple artefact. In het proefschrift wordt een analyse van het mechanisme achter dit ripple artefact gepresenteerd. De zichtbaarheid van de overgangen tussen plakken wordt extra benadrukt door de signaalverplaatsingen in de frequentiecoderingsrichting.
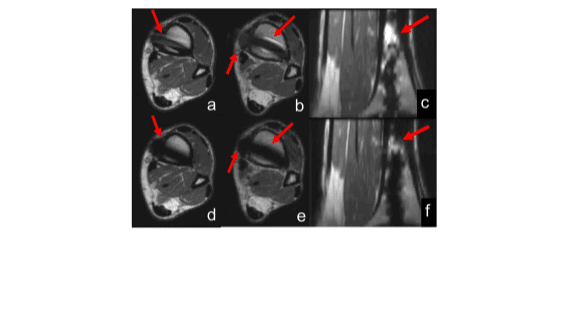
Het gebruik van bredere overlappende plakselecties zorgt voor vloeiender overgangen tussen de plakselecties, en reduceert het ripple artefact aanzienlijk (Figuur 9 en 10). Zowel de analyse van het mechanisme achter het ripple artefact en de benadering om het artefact te reduceren zijn geverifieerd met behulp van MRI-simulaties en fantoomexperimenten.
Prototype
Om te evalueren of met MSI technieken uitgebreid met ORS (ORS-MSI) metaalartefacten naar tevredenheid kunnen worden aangepakt, is tijdens het promotieonderzoek een software-prototype gebouwd met de MSI en ORS functionaliteit. Dit prototype is gebaseerd op software die draait op een klinische Philips MRI-scanner, om zo installatie van het prototype op Philips MRI-scanners in ziekenhuizen mogelijk te maken. Het proefschrift beschrijft welke klinische eisen (aangeleverd door orthopeden en radiologen) en technische eisen de standaard hebben gezet voor het prototype, zodat de verschillende aspecten van de functionaliteit konden worden geëvalueerd, waaronder correctie, toepasbaarheid, snelheid en gebruiksvriendelijkheid.
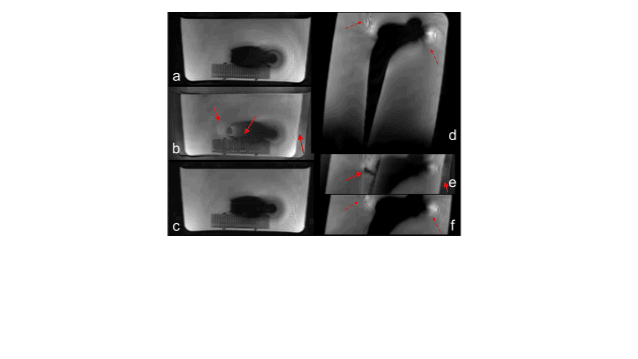
Met behulp van fantoomexperimenten is gecontroleerd of de functionaliteit van het prototype resulteert in de correctie van geometrische vervormingen en afwijkingen in signaalintensiteit die mag worden verwacht op basis van de theorie. Een validatiestudie of de bereikte artefactreductie voldoet aan de klinische behoefte toonde aan dat een goede visualisatie op slechts een halve centimeter afstand van een titanium heupimplantaat mogelijk is (Figuur 11).
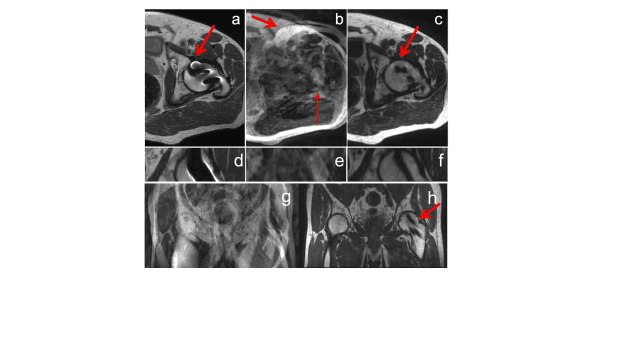
Bij een roestvrijstalen heupimplantaat werd niet aan de klinische behoefte voldaan (Figuur 12): de afmeting van het artefact varieerde per locatie, en was aanzienlijk kleiner dan een halve centimeter in de buurt van de heupsteel maar groter dan een centimeter in de buurt van de kop van het implantaat.
Discussie en Conclusie
Niettemin was het artefact aanzienlijk gereduceerd met behulp van de functionaliteit van het prototype in vergelijking met conventionele scantechnieken. Van artefacten nabij massieve roestvrijstalen implantaten mag worden verwacht dat dit de meest uitdagende artefacten zijn om te reduceren. Veel andere implantaten, met kleinere afmeting of gemaakt van andere materialen, zullen kleinere artefacten veroorzaken en voor die implantaten biedt ORS-MSI voldoende artefactreductie binnen klinisch haalbare scantijden. In alle experimenten werden metaalartefacten nooit versterkt door het gebruik van ORS-MSI.
De beschreven methoden voor de verificatie en validatie van het proefontwerp omvatten simulaties en fantoom- en vrijwilligerexperimenten. Evaluatie van de functionaliteit op patiënten in de klinische praktijk is nodig om het klinische nut van de techniek verder aan te tonen. Aan de klinische evaluatie wordt gewerkt. De eerste resultaten tonen voldoende klinisch nut om productontwikkeling van de nieuwe functionaliteit aan te bevelen. Daarmee zal de voorgestelde ORS-MSI functionaliteit voor artefactreductie nabij metalen implantaten binnenkort beschikbaar worden als commercieel product en evaluatie en diagnose van weefsel mogelijk maken in klinisch haalbare scantijden dichter bij metalen implantaten dan elke andere momenteel beschikbare techniek.
Dit artikel is een aangepaste versie van de samenvatting van het proefschrift: Metal Implant Artifact Reduction in Magnetic Resonance Imaging, door Chiel den Harder. Chiel is in januari 2015 gepromoveerd aan de Technische Universiteit Eindhoven.