De blootstelling aan grote hoeveelheden klinische alarmen kan leiden tot alarmmoeheid. Een mogelijk gevolg is het missen van een kritisch alarm, of een vertraagde respons op een kritisch alarm. Dit kan uitlopen op een ernstig ongewenst voorval, oftewel een Serious Adverse Event (SAE) [1,2]. Recente artikelen op MT-Integraal gingen in op alarmdistributie onder de Medical Device Regulation (MDR) [3] en veiligheidsaspecten van stillere alarmering [4].
Dit artikel presenteert concrete technieken om alarmveiligheid te verbeteren en bevat objectieve meetmethoden om de effectiviteit ervan te beoordelen. Verder wordt een stappenplan gepresenteerd om continu te blijven verbeteren.
Alarmdistributie kan daar deel van uitmaken. Enkele aandachtspunten en valkuilen worden toegelicht. De rijkste oplossingen hebben hierbij niet altijd het grootste effect. Ultieme doelen zijn een stille zorgomgeving en een optimale inzet van alle informatie ten behoeve van alarmpreventie.
Hoe kan ik alarmmoeheid objectief meten?
Er is geen eenduidige en directe objectieve vaststelling van alarmmoeheid. Wel zijn er twee veelvoorkomende objectieve maatstaven te vinden in de literatuur:
- De alarm rate, bijvoorbeeld het aantal alarmen per patiënt per uur.
- De responstijd of alarmduur
Het is algemeen bekend dat het merendeel van de alarmen vals is, of klinisch irrelevant. Schattingen lopen uiteen van bijvoorbeeld 72-99% [2] tot 80-99% [5].
Daarom is het reduceren van het aantal valse of irrelevante alarmen het eerste speerpunt. Dan neemt de kans toe dat een alarm relevant is en wordt de responstijd naar verwachting korter [5-8]. Een snellere respons op kritische alarmen vergroot de veiligheid, door de kans op een SAE te verkleinen. Sommige studies meten de responstijd met menselijke waarnemers, andere met videocamera’s [9].
Echter, vooral zichtbare observatiemethoden kunnen in meer of mindere mate de meting beïnvloeden [8,10]. Een alternatieve maatstaf voor de responstijd is de alarmduur [7,11-15]. De alarmduur kan onzichtbaar en objectiever vastgesteld worden via de communicatieprotocollen van de medische hulpmiddelen of via de logs van de devices zelf. Soms wordt een alarm als irrelevant geclassificeerd als bijvoorbeeld de responstijd meer dan 90 seconden bedraagt, omdat er kennelijk onvoldoende reden zou zijn geweest voor een snelle respons [9]. Het wordt echter afgeraden om het ontbreken van een respons te interpreteren als een irrelevant alarm [10]. Immers, dat is juist een potentieel gevolg van alarmmoeheid.
Het kijken door een raam of deuropening als respons beschouwen [16], is eveneens discutabel. Naast objectieve maatstaven, worden subjectieve vragenlijsten regelmatig toegepast [9,17,18]. Deze spelen in op de perceptie, die niet altijd in overeenstemming is met objectieve metingen. Bijvoorbeeld kan op een afdeling het gevoel heersen dat er minder belangrijke alarmen genegeerd worden na een interventie, terwijl de objectief gemeten duur van belangrijke alarmen niet significant gereduceerd is [19]. Tevens kan het geluidsniveau objectief worden gemeten [15]. Geluid kan bijdragen aan delier, waardoor ligduur, kosten, morbiditeit en mortaliteit kunnen toenemen [20,21].
De incidentie van delier kan oplopen tot 70 of 80% bij IC-patiënten [21] of 85% bij mechanische beademing [20]. Merk hierbij op dat geluiden niet uitsluitend van alarmen afkomstig zijn.
Stappenplan: alarmveiligheid vaststellen en verbeteren
Er zijn enkele uitstekende recepten in omloop om alarmveiligheid te verbeteren, met diverse gemeenschappelijke ingrediënten [22,23]. Dit leidt tot het volgende stappenplan:

De stappen
1. Begin met een nulmeting. Meet de aantallen alarmen per patiënt per uur, de alarmduur, de vitale parameters en leg instellingen vast. Kijk welke apparaten de meeste alarmen genereren en welke alarmcondities het vaakst voorkomen. Neem bij infuuspompen ook de medicatie mee. Geluidsmetingen zijn een meerwaarde. Beperk de metingen niet alleen tot patiëntmonitoren. Pompen en ventilatoren samen kunnen meer alarmen van hoge prioriteit opleveren dan patiëntmonitoren.
2. Stel kritische alarmen vast. Bepaal welke alarmen daadwerkelijk kritisch zijn: welke alarmcondities hebben een hoge prioriteit én vereisen een onmiddellijke respons? Stel hiervoor de maximaal acceptabele alarmduur vast. Dit is mede afhankelijk van de zorgomgeving en het type patiënt, bijv. een IC voor volwassenen of neonatologie. Bepaal eveneens de irrelevante of non-actionable alarmcondities, bijvoorbeeld condities waarvoor geen behandeling is opgenomen in de richtlijnen, als deze een minimale duur niet overschrijden [24]. Deze alarmcondities kunnen desondanks wel interessant zijn voor een EPD of PDMS.
3. Betrek een multidisciplinair team met de juiste personen: verpleegkundigen, artsen, afdelingshoofden, klinische fysici, klinische informatici, biomedische technologen, medisch-technici, ICT’ers, managers en andere belanghebbenden in uw eigen organisatie. Probeer ook fabrikanten mee te nemen.
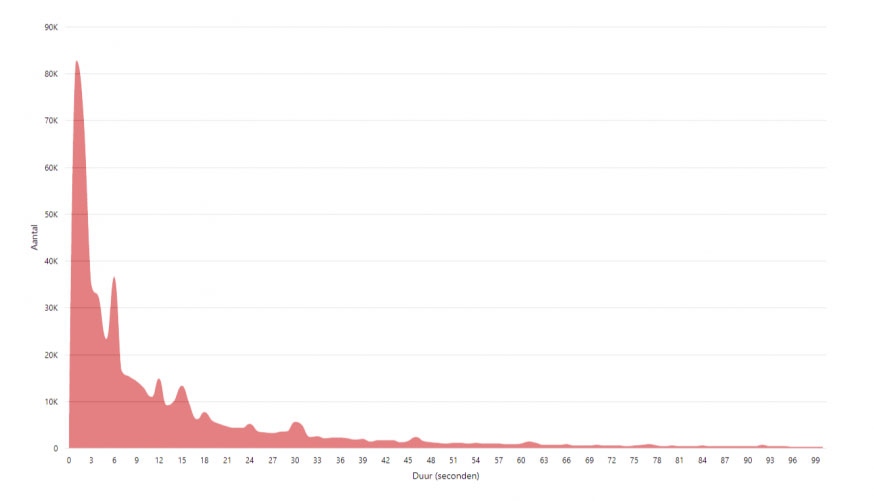
4. Analyseer de data en sta daarbij open voor verrassingen. Laat de data leidend zijn, volg niet alleen hypotheses. Analyseer van alle devices tenminste de alarmen, vitale parameters en instellingen. Merk voor de analyse op dat de verdeling van de alarmduur doorgaans scheef is (zie figuur 1 hieronder). Methoden voor normale verdelingen kunnen hierbij zelfs leiden tot een betrouwbaarheidsinterval met een negatieve responstijd [12]; de spreekwoordelijke alarmbellen zouden dan moeten gaan rinkelen.
5. Stel meetbare doelen en bepaal maatregelen. Bepaal maatregelen en deel de onderliggende doelstellingen met de afdeling. Maak een plan hoe de effectiviteit getoetst kan worden en welke parameters daarvoor vereist zijn. Oftewel, maak het doel meetbaar. Focus op vitale parameters en instellingen.
Veel alarmen vinden hun oorsprong in afwijkende vitale parameters of instellingen. Interventies zijn enerzijds gericht op beleid, anderzijds technisch van aard, met wisselend succes [15]. Beleid richt zich bijvoorbeeld op alarmgrenzen, de bevestiging van elektrodes of patiëntafhankelijke instellingen. Aan de technische kant zijn er alarm-algoritmes, bewuste vertragingen en multiparametric smart alarms [19,25]. Waak ervoor dat er geen echt alarm gemist wordt [15]. Relatief weinig alarmreductie-oplossingen zijn daadwerkelijk bewezen [6].
Het is wel duidelijk dat relatief veel alarmen een korte duur hebben (zie de scheve verdeling hieronder). Met bewuste vertragingen kan een alarm zichzelf corrigeren, of door een verpleegkundige ter plekke afgehandeld worden, voordat het eventueel gedistribueerd wordt. De maximale duur van een veilige vertraging hangt vanzelfsprekend af van de alarmconditie en de omgeving [5,7,12-15,26].
Verschillende oplossingen zijn gericht op hele specifieke, kritische alarmcondities. Deze kritische alarmcondities komen naar verhouding weinig voor. De grootste potentiële alarmreductie zit daarom juist in de niet-kritische alarmcondities. Als deze eerste en grootste reductie gerealiseerd is, dan zou het perspectief op de resterende alarmen totaal anders kunnen zijn.
6. Bepaal de effectiviteit van de maatregelen en voer nodige aanpassingen door. Per maatregel kan vooraf een hypothetische reductie bepaald worden op basis van eerdere metingen. In de praktijk pakt deze reductie waarschijnlijk anders uit, vanwege onvoorziene neveneffecten op bijvoorbeeld de verpleegkundige of de patiënt. Toets daarom de effectiviteit aan de verwachting. En stel maatregelen eventueel bij.
7. Leg resultaten vast. Documenteer alle voorgaande stappen, inclusief de resultaten. Blijf meten om continu te verbeteren en te controleren of verbeteringen gehandhaafd blijven.
Integratie en alarmdistributie
Steeds meer worden eenpersoonskamers gebruikt, die bovendien steeds vaker afgesloten kunnen worden. Om de verpleegkundige te attenderen op een alarm, wordt veilige alarmdistributie een noodzaak. Een bronapparaat deelt een alarm via een eigen communicatieprotocol met een zogenoemde integrator [27]. Een integrator kan specialistische functionaliteit bevatten voor het uitfilteren van irrelevante alarmen, van verschillende apparaten van diverse vendors tegelijk.
Daarnaast dient een integrator meestal vitale parameters en instellingen door te sturen naar een elektronisch patiëntendossier (EPD) of een patient data management system (PDMS). Specifieke alarmen zouden bovendien aangeboden kunnen worden als bijzondere gebeurtenis aan hetzelfde EPD of PDMS. De integrator stuurt gefilterde alarmen bij voorkeur door naar een gedistribueerd alarmdistributiesysteem met bevestiging (confirmation) van de verpleegkundige (CDAS). Een communicator (of handheld) dient vervolgens de verpleegkundige te voorzien van de relevante informatie. Ook als er meerdere gelijktijdige alarmcondities op hetzelfde bed zijn, of op verschillende bedden.
Aan de andere kant hoeft een verpleegkundige die naast een patiënt staat, niet dubbel geïnformeerd te worden over alarmen afkomstig van deze patiënt. Risico-georiënteerde richtlijnen zijn beschikbaar in standaarden en technical reports [27,28]. Deze bespreken de verantwoordelijkheden van zowel fabrikanten als de responsible organization in een ziekenhuis. O.a. moeten over de hele alarmketen connecties bewaakt worden.
Valkuilen alarmdistributie
Alarmdistributie kan bijdragen aan een oplossing om alarmmoeheid te reduceren en de patiëntveiligheid te vergroten. Dit is echter nog geen vanzelfsprekendheid. Een valkuil is het doorsturen van grote hoeveelheden alarmen, verrijkt met extra informatie, om de verpleegkundige op afstand te laten beoordelen welk alarm relevant is. Echter, in de kritische zorg kunnen er gemiddeld tientallen alarmen per uur per bed optreden, wat een onwerkbare situatie zou opleveren. Het gemiddelde aantal voor een individuele patiënt kan zelfs boven de 200 alarmen per uur uitvallen [24].
Een eerste stap is het terugdringen van het aantal irrelevante alarmen. Hier valt de grootste winst te behalen. Het doel is dat een verpleegkundige voor de resterende alarmen kan beoordelen welke patiënt zorg nodig heeft en met hoeveel spoed. Hiervoor moet het aantal doorgestuurde alarmen hanteerbaar zijn. Bovendien moeten alarmen voorzien zijn van tenminste de essentiële informatie: locatie (bed), apparaat, alarmconditie en prioriteit.
Overweeg uitsluitend om alarmen te verrijken met andere informatie, als deze de patiëntveiligheid ten goede komt. Waveforms zijn bijvoorbeeld een veel gehoorde wens van verpleegkundigen [9], maar het effect ervan wordt betwijfeld totdat de veiligheid ervan bewezen is [13]. Het kan de verpleegkundige er namelijk ten onrechte van weerhouden om naar de patiënt te gaan bij een alarm. De waveform heeft daarnaast een potentiële vertraging [29].
Het is meestal ook niet exact bekend op welk tijdstip een alarmconditie is vastgesteld t.o.v. de waveform. Is één waveform op een relatief klein scherm van een handheld bovendien toereikend voor een juiste inschatting, in een potentieel kritische situatie? En welke dan?
In de praktijk kan zelfs een standaardset van 8 waveforms op een groot scherm van een patiëntmonitor als onvoldoende beschouwd worden. Bijvoorbeeld wanneer een tweede ICP-waveform gewenst is [30]. De bepalende waveform is niet telkens dezelfde, maar afhankelijk van de situatie [24]. Veel valse alarmen worden ook niet veroorzaakt door een slechte signaalkwaliteit, als het bijvoorbeeld om aritmie gaat. Let tenslotte op de ergonomische principes uit de Medical Device Directive (MDD) en MDR , die van toepassing zijn op amplitude, schaal en eenheden.
Apparaatprotocollen
De kracht en de mogelijkheden van een volledige alarmdistributieketen zijn in belangrijke mate afhankelijk van de input uit de communicatieprotocollen van de bedzijdige medische apparaten. Deze zijn helaas niet gestandaardiseerd of geharmoniseerd over verschillende fabrikanten, of in beperkte mate. Let op de protocoleigenschappen bij de vervanging van apparatuur. Aspecten van belang zijn:
- Intended use en classificering
- De aanwezigheid van alle alarmcondities in het protocol, inclusief prioriteit
- Hoe vaak worden vitals en settings verstuurd
- Wat is de latency (de onbewuste vertraging)
- Wordt stille alarmering ondersteund, d.w.z. geen geluid bij de patiënt, maar wel bij de verpleegkundige Kan een alarmdistributiesysteem terugkoppelen naar de bron
- Wordt de standby-modus van een apparaat doorgegeven, evenals het onderdrukken van een alarm
- De kwaliteit en accuraatheid van alarmdetectie-algoritmes
- Ondersteunt het apparaat de detectie van verbroken verbindingen
- Firmware upgrades
- Het type connectie (serieel, TCP/IP, gateway).
Conclusies en toekomstvisie
Alarmveiligheid en alarmmoeheid zijn onlosmakelijk met elkaar verbonden. Objectieve maatstaven zijn de alarm rate en de alarmduur van kritische alarmen in het bijzonder.
Begin zo vroeg mogelijk met een nulmeting, om de alarmveiligheid vast te stellen. Neem niet alleen patiëntmonitoren mee, maar ook andere devices. De data-gedreven analyse van alleen al de tussenresultaten zal naar verwachting bijdragen aan een verhoogde betrokkenheid van alle verschillende disciplines.
De grootste potentiële alarmreductie zit in de niet-kritische alarmcondities. Het verrijken van alarminformatie op handhelds is daarom niet de aanbevolen eerste stap, omdat de verpleegkundige hiermee effectief als alarmfilter zou gaan fungeren. Filter de irrelevante condities er juist zoveel mogelijk uit vóórdat ze bij een verpleegkundige aankomen. Met een hanteerbaar aantal doorgestuurde alarmen kan de verpleegkundige bepalen welke patiënt zorg nodig heeft en hoe snel.
Met de aandachtspunten van alarmveiligheid in het achterhoofd, moeten we openstaan voor innovatieve oplossingen. Wat op de ene afdeling niet werkt, kan op de andere afdeling wel werken. En vice versa. Stel meetbare doelen en bepaal de effectiviteit van de maatregelen. Patiëntveiligheid staat voorop, in het bijzonder de respons op kritische alarmen. Waak ervoor dat er geen echt alarm gemist wordt. Let op alle verschillende protocoleigenschappen, die eveneens een belangrijke schakel in de keten vormen.
Een ultiem doel is het preventief of diagnostisch benutten van alle beschikbare gegevens: near real-time alarmen en vitale waarden van de verschillende bedzijdige apparaten. Hierin kunnen diagnoses en andere patiënt-specifieke gegevens tevens een rol spelen. Mogelijk kan de informatie zelfs meewegen in de bepaling van de capaciteitsvraag. Een ander doel is de stille zorgomgeving. Met geschikte apparaten en een betrouwbare alarmdistributie wordt dit doel realiseerbaar.
Met sommige van de modernste devices zal terugkoppeling door de gehele keten mogelijk worden, tot aan de bron. De stilte in combinatie met een veiligere omgeving komt uiteindelijk niet alleen ten goede aan patiënten, maar ook aan zorgverleners [25].
Referenties
[1] FDA Patient Safety News – Show #106, January 2011
[2] M Funk et al (2014). Attitudes and practices related to clinical alarms. American Journal of Critical Care, 23(3), e9-e18.
[3] Cindy Egberts, 2019 [LINK]
[4] Carola van Pul, 2015 [LINK]
[5] M Cvach (2012). Monitor alarm fatigue: an integrative review. Biomedical instrumentation & technology, 46(4), 268-277.
[6] Bach et al. “Managing alarm systems for quality and safety in the hospital setting.” BMJ Open Qual 7.3 (2018).
[7] Görges et al., 2009. Improving alarm performance in the medical intensive care unit using delays and clinical context. Anesthesia & Analgesia, 108(5), 1546-1552.
[8] Johnson et al., 2017. Alarm safety and alarm fatigue. Clinics in perinatology 44.3: 713-728.
[9] Joshi et al., 2017. The heuristics of nurse responsiveness to critical patient monitor and ventilator alarms in a private room neonatal intensive care unit. PloS one 12.10
[10] Ruppel et al, 2018b. Measurement of physiological monitor alarm accuracy and clinical relevance in intensive care units.” American Journal of Critical Care 27.1: 11-21.
[11] Belteki & Morley, 2018. Frequency, duration and cause of ventilator alarms on a neonatal intensive care unit. Archives of Disease in Childhood-Fetal and Neonatal Edition 103.4 (2018): F307-F311.
[12] Bonafide et al., 2017. Video analysis of factors associated with response time to physiologic monitor alarms in a children’s hospital. JAMA pediatrics 171.6: 524-531.
[13] Cvach et al., 2014. Use of pagers with an alarm escalation system to reduce cardiac monitor alarm signals. Journal of nursing care quality 29.1: 9-18.
[14] Paine et al., 2016. Systematic review of physiologic monitor alarm characteristics and pragmatic interventions to reduce alarm frequency. Journal of hospital medicine 11.2: 136-144.
[15] Winters et al., 2018. “Technological distractions (part 2): a summary of approaches to manage clinical alarms with intent to reduce alarm fatigue.” Critical care medicine 46.1: 130-137.
[16] Bonafide et al., 2015. Association between exposure to nonactionable physiologic monitor alarms and response time in a children’s hospital. Journal of hospital medicine, 10(6), 345-351.
[17] Ashrafi et al., 2017. Designing an Alarm Fatigue Assessment Questionnaire: Evaluation of the Validity and Reliability of an Instrument. Journal of Critical Care Nursing 10.4.
[18] Torabizadeh et al., 2017. A nurses’ alarm fatigue questionnaire: development and psychometric properties. Journal of clinical monitoring and computing 31.6: 1305-1312.
[19] Ruppel et al., 2018. Testing physiologic monitor alarm customization software to reduce alarm rates and improve nurses’ experience of alarms in a medical intensive care unit. PloS one 13.10.
[20] Ibrahim et al., 2018. Delirium in the cardiac intensive care unit. Journal of the American Heart Association 7.4.
[21] Xie et al., 2009. Clinical review: The impact of noise on patients’ sleep and the effectiveness of noise reduction strategies in intensive care units. Critical Care 13.2: 208.
[22] Johns Hopkins, 2012. Association for the Advancement of Medical Instrumentation (AAMI) Foundation/Healthcare Technology Safety Institute (HTSI). Using Data to Drive Alarm System Improvement Efforts, The Johns Hopkins Hospital Experience. http://www.aami.org/htsi/SI_Series/Johns_Hopkins_White_Paper.pdf
[23] Alarm compendium, 2015. Clinical Alarm Management Compendium, 2015
[24] Drew et al., 2014. Insights into the problem of alarm fatigue with physiologic monitor devices: a comprehensive observational study of consecutive intensive care unit patients. PloS one, 9(10).
[25] Hravnak et al., 2018. A call to alarms: Current state and future directions in the battle against alarm fatigue. Journal of electrocardiology.
[26] Borowski et al., 2011. Medical device alarms. Biomedizinische Technik/Biomedical Engineering, 56(2), 73-83.
[27] IEC TR 80001-2-5. Application of risk management for IT-networks incorporating medical devices – Part 2-5: Application guidance – Guidance on distributed alarm systems, Edition 1.0 2014-12
[28] IEC 60601-1-8. Medical electrical equipment – Part 1-8: General requirements for basic safety and essential performance – Collateral standard: General requirements, tests and guidance for alarm systems in medical electrical equipment and medical electrical systems, Edition 2.1, 2012-11
[29] Fernández-López, 2011. Remote vital signs monitoring based on wireless sensor networks (Doctoral dissertation).
[30] Sowan et al., 2017. Nurse competence on physiologic monitors use: toward eliminating alarm fatigue in intensive care units. The open medical informatics journal, 11, 1