Inleiding
Voor het aantonen van coronaire hartziekten of voor het beoordelen van de ernst van bekend CAD, kan de doorbloeding van het myocard in beeld gebracht worden (myocard perfusion imaging, MPI). Op deze niet-invasieve wijze wordt inzicht verkregen of en in welke mate een eventuele stenose leidt tot verminderde perfusie van het myocard. Tevens kan aan de hand van de beelden vastgesteld worden of er in delen van de hartwand sprake is van een ernstig verlaagde doorbloeding (ischemie) of zelfs afwezige doorbloeding (infarct). Bij myocard perfusie onderzoek is het gebruikelijk om de doorbloeding van het hart af te beelden onder normale en onder verhoogde zuurstofbehoefte van de hartspiercel, bijvoorbeeld door middel van de combinatie van een rustonderzoek en een inspanningsonderzoek.
SPECT
De meest voorkomende vorm van myocard perfusie imaging is SPECT (single photon emission computed tomography) onderzoek dat uitgevoerd wordt met behulp van een gammacamera. Doorgaans wordt hierbij een met radioactief technetium (Tc-99m) gemerkt preparaat gebruikt (sestamibi of tetrofosmine), dat radiofarmacon of tracer wordt genoemd. Tc-99m is een γ-emitter met een halfwaardetijd van 6 uur. Voor zowel het rustonderzoek als het inspanningsonderzoek krijgt een patiënt een injectie met de tracer en wordt met behulp van een gammacamera een SPECT acquisitie verricht [1]. Doordat de camerakoppen om de patiënt roteren, kunnen vervolgens driedimensionale reconstructies gemaakt worden, zodat het hart vanuit alle richtingen maar ook langs verschillende doorsneden bekeken kan worden. Door gebruik te maken van ECG triggering tijdens de acquisitie kunnen bovendien gated reconstructies gemaakt worden. Hierbij worden afzonderlijke reconstructies gemaakt van deelfasen van de hartslag, die vervolgens als filmpje kunnen worden afgespeeld. Aan de hand hiervan kan onder andere de linkerventrikel ejectiefractie (LVEF) berekend worden en kunnen regionale wandbewegingen beoordeeld worden. Voorafgaand aan de acquisitie van het inspanningsonderzoek verricht de patiënt een inspanningstest op een fietsergometer of loopband. Tegen het einde van deze inspanningstest, vindt de injectie van activiteit plaats en zal de tracer opgenomen worden door onder andere de hartspier. Vervolgens wordt er gewacht (30-45 minuten) totdat de overige activiteit uit het lichaam verdwenen is, waarna de patiënt pas plaatsneemt onder de gammacamera. Doordat het enige tijd duurt voordat de Tc-99m activiteit ook uit de hartspier verdwenen is, dient er enkele uren gewacht te worden tussen het uitvoeren van het rustonderzoek en het uitvoeren van het inspanningsonderzoek. Als gevolg hiervan is de patiënt een groot deel van de dag aanwezig in het ziekenhuis, of worden de twee fasen van het onderzoek op twee opeenvolgende dagen verricht.
Isotopenproductie
Technetium is een van de meest gebruikte radioactieve stoffen voor medische beeldvormende diagnostiek. Ziekenhuizen maken gebruik van speciale vaatjes die het isotoop molybdeen (Mo-99) bevatten, dat door radioactief verval Tc-99m produceert. Mo-99 wordt verkregen door splijting van verrijkt uranium (U-235) in een kernreactor. Wereldwijd wordt in de medische behoefte aan Tc-99m voorzien door een vijftal kernreactoren. Wanneer meer dan één van deze reactoren gelijktijdig, wegens onderhoud of technische problemen, langere tijd buiten gebruik is, dreigt er een tekort aan medische isotopen. Sinds 2008 is hier meerdere malen sprake van geweest, waardoor de vraag naar alternatieven sterk gegroeid is [2]. Zo heeft Medisch Centrum Alkmaar sinds 2013 als eerste niet-academisch ziekenhuis in Nederland een eigen cyclotron in gebruik voor de productie van PET (positron emission tomography) isotopen [3]. Dit stelt het ziekenhuis in staat om verschillende onderzoeken die voorheen met een gammacamera verricht werden, nu met een veel gevoeligere PET/CT scanner uitvoeren zonder daarvoor afhankelijk te zijn van de beschikbaarheid van kernreactoren. Voor myocard perfusie onderzoek bestaat er echter ook een alternatief waarvoor geen on-site cyclotron nodig is, namelijk PET onderzoek met radioactief rubidium (Rb-82) [4]. Het kortlevende isotoop Rb-82 (β-plus emitter met een halfwaarde tijd van 75 seconden) wordt verkregen uit een generator door verval van radioactief strontium (Sr-82). Sr-82 kan geproduceerd worden in grotere cyclotrons en is voldoende langlevend (halfwaarde tijd van 25.4 dagen) om getransporteerd te worden.
Rubidium
In de Verenigde Staten wordt rubidium sinds het einde van de jaren ‘80 toegepast voor myocard perfusie onderzoek. Rubidium is echter niet als geneesmiddel geregistreerd in Europa en mag, mits aan bepaalde voorwaarden wordt voldaan, enkel op artsenverklaring toegepast worden. Pas sinds enkele jaren en op zeer kleine schaal hebben in de VS geregistreerde generatoren daadwerkelijk hun intrede gedaan in Europese landen, waaronder het Verenigd Koninkrijk, Denemarken en zeer recent ook Nederland. In 2006 bleek het echter niet mogelijk te zijn een Amerikaanse generator te importeren naar Nederland. Nucleair Geneeskundige Roel Claessens van het Jeroen Bosch Ziekenhuis (JBZ) besloot daarop om zelf een generator te ontwikkelen. Hierbij voerde hij tegelijkertijd een aantal verbeteringen door ten opzichte van de commerciële generatoren. Zo wordt in de generator van Claessens real-time een dynamische calibratie van de patiëntdosering toegepast. Verder is na één maand gebruik een generator te zwak om nog ingezet te worden en dient deze normaal gesproken vervangen te worden. Claessens heeft zijn generator echter zo ontworpen dat deze bijgeladen kan worden met een kleinere hoeveelheid strontium. De generator kan daarmee weer op oorspronkelijke sterkte gebracht worden en hoeft niet vroegtijdig vervangen te worden. De technische ontwikkeling van de generator verliep voorspoedig, echter daarmee stonden niet automatisch alle lichten op groen voor de klinische toepassing van rubidium. De Inspectie voor de Gezondheidszorg (IGZ) eiste dat de rechtspersoon die de generator exploiteert beschikt over een fabrikanten vergunning, wat onder andere inhield dat de laboratorium faciliteiten in het Jeroen Bosch Ziekenhuis gecertificeerd dienden te worden volgens de GMP (Good Manufacturing Practice) standaarden die gelden voor farmaceutische bedrijven. Uiteindelijk werd in april 2012 het eerste Rb-82 PET myocard perfusie onderzoek verricht in het JBZ en sindsdien worden per jaar meer dan 1000 patiënten onderzocht met de generator van Claessens.
CardioPET
Bij een PET scanner bevinden zich grote aantallen scintillatiekristallen en detectorelementen geordend in ringen rondom de patiënt. Het fysische principe van een PET scan is gebaseerd op de gelijktijdige detectie van twee in tegenovergestelde richting uitgezonden annihilatie fotonen, die vrijkomen wanneer een uitgezonden positron op een elektron botst. Hierdoor kent PET een hogere spatiële resolutie dan SPECT en leidt een CT gebaseerde verzwakkingscorrectie tot betrouwbaardere resultaten dan bij SPECT [5]. Daarnaast heeft een PET scanner een hogere gevoeligheid dan een gammacamera. Hierdoor is het mogelijk om beelden in kortere tijd te acquireren, wat een vereiste is bij het gebruik van kortlevende isotopen zoals Rb-82. Door de korte halfwaardetijd van 75 seconden, vindt de toediening van rubidium pas plaats op het moment dat de patiënt zich al in de scanner bevindt. Hierdoor is het niet mogelijk om de patiënt een fysieke inspanningstest te laten verrichten op een fietsergometer of loopband. In plaats daarvan wordt voor het inspanningsonderzoek gebruik gemaakt van farmacologische stress. De patiënt krijgt hierbij een medicijn toegediend, bijvoorbeeld adenosine dat zorgt voor verwijding van de coronaire bloedvaten. Een nadeel van het gebruik van adenosine zijn eventuele bijwerkingen zoals benauwdheid en een drukkend gevoel op de borst. De werking van adenosine is echter kort, waardoor eventuele bijwerkingen ook gauw weer verdwijnen. Hierdoor en door de korte halveringstijd van Rb-82 is het mogelijk om vrij snel na het inspanningsonderzoek het rustonderzoek uit te voeren. Inclusief patiëntvoorbereiding, waarbij onder andere ECG elektrodes geplakt worden, wordt het totale myocard perfusie onderzoek doorgaans binnen één uur uitgevoerd. Ten opzichte van SPECT onderzoek betekent dit een significante verkorting van de verblijfstijd van de patiënt in het ziekenhuis. Daarnaast is de stralingsbelasting voor de patiënt ten gevolge van Rb-82 PET onderzoek circa 3 keer zo laag als bij Tc-99m SPECT onderzoek [6]. Met het oog op de stralingsbelasting van de patiënt is het wel noodzakelijk om dagelijks kwaliteitscontroles uit te voeren aan de rubidium generator. Door middel van deze controle wordt vastgesteld dat er geen noemenswaardige hoeveelheden strontium vrijkomen bij de elutie van rubidium. Strontium (Sr-82 en Sr-85) heeft namelijk een veel langere halveringstijd en zou reeds bij het vrijkomen van kleine hoeveelheden leiden tot een meetbare restactiviteit in de patiënt.
Reconstructies
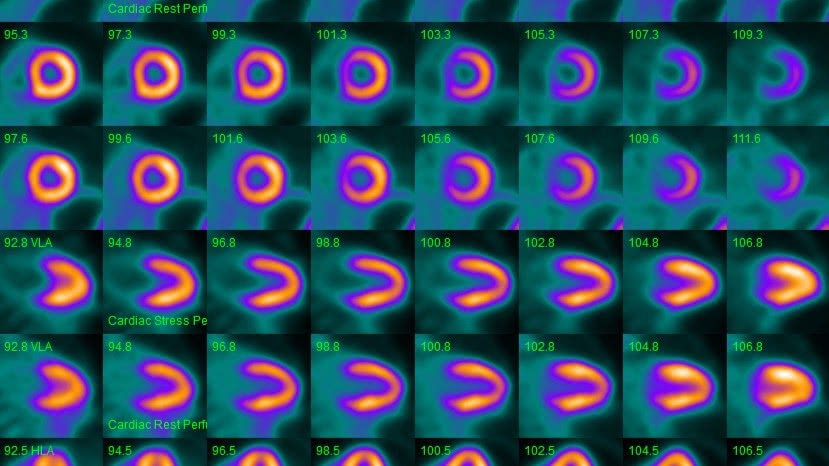
Een volledig Rb-82 myocard perfusie onderzoek bestaat uit een CT-scan van de hartregio van de patiënt en twee PET-acquisities, voor respectievelijk het inspanningsonderzoek en het rustonderzoek, van één bedpositie. De PET acquisitieduur bedraagt 7 minuten en start op het moment dat de eerste infusie van rubidium naar de patiënt plaatsvindt. Data acquisitie vindt plaats in listmode, wat inhoudt dat alle ruwe PET data opgeslagen worden. Deze PET data kunnen dan achteraf herschikt worden in zogeheten sinogrammen die vervolgens gereconstrueerd worden tot beelden. Op deze wijze kunnen verschillende typen reconstructies gemaakt worden: statische beelden, op basis waarvan de doorbloeding van het hart visueel beoordeeld wordt (figuur 1), maar ook dynamische beelden, aan de hand waarvan de perfusie gekwantificeerd kan worden. Ook wordt er een snelle statische reconstructie gemaakt op basis waarvan uitlijning van de PET dataset met de CT dataset plaatsvindt zodat de CT data gebruikt kunnen worden voor verzwakkingscorrectie van de overige reconstructies. Doordat er gebruik gemaakt wordt van ECG triggering tijdens de acquisitie is het bovendien mogelijk om gated reconstructies te maken, aan de hand waarvan de linkerventrikel ejectiefractie bepaald kan worden. Op deze wijze resulteert een acquisitie van 7 minuten in een grote hoeveelheid beeldinformatie en de reconstructie ervan neemt een veelvoud van de acquisitietijd in beslag. Figuur 2 geeft een overzicht van de verschillende beeldenseries die worden gegenereerd en de reconstructietechniek die hierbij wordt toegepast.
Flow reserve
Naast reeds genoemde voordelen als lagere stralingsbelasting en kortere doorlooptijd van het onderzoek, biedt Rb-82 PET ook nieuwe informatie die niet verkregen kan worden met SPECT onderzoek. Doordat de toediening van rubidium plaats vindt terwijl de patiënt zich in de PET scanner bevindt, kan het instromen van Rb-82 in de rechter en vervolgens linker kamer van het hart afgebeeld worden. Dit instromen, het weer uit spoelen en de daarop volgende opname van rubidium in het myocard is goed te zien in de dynamische beelden. Door in deze beelden de contouren van het hart te detecteren en de hartwand op te delen in kleine volume elementen, kan voor elk van deze elementen het verloop van opgenomen activiteit in de tijd bepaald worden (time-activity curve, TAC). Verder kan met behulp van een volume element in het linker ventrikel het verloop van de activiteit in het instromende bloed in de tijd bepaald worden (blood input function, BIF). Vervolgens kan softwarematig de overdracht van input functie naar weefsel TAC gemodelleerd worden. Aan de hand van de fit parameters uit dit model, kan vervolgens de flow naar het betreffende deel van het myocard bepaald worden. Door dit zowel voor het rustonderzoek als voor het inspanningsonderzoek te doen, kan de relatieve toename in de bloedvoorziening naar het myocard (coronary flow reserve, CFR) gekwantificeerd worden (figuur 3). Op deze wijze kan vastgesteld worden in welke mate een eventuele stenose daadwerkelijk een belemmering vormt voor de toevoer van bloed naar de hartspier. De absolute kwantificering van flow en flow reserve op basis van Rb-82 PET myocard perfusie onderzoek heeft daarmee potentiële meerwaarde binnen de diagnostiek van coronaire hartziekten [7].
[1] Barneveld PC en Urk, van P, Aanbevelingen Nucleaire Geneeskunde 2007, 2007, pp 120-125;
[2] Thomas GS en Maddahi J, The technetium shortage, J Nucl Cardiol, 2010, vol 17, pp 993-8;
[3] Medisch Centrum Alkmaar, Cyclotron in gebruik, 2013, geraadpleegd op 30 oktober 2014;
[4] BA Mc Ardle et al, Does rubidium-82 PET have superior accuracy to SPECT perfusion imaging for the diagnosis of obstructive coronary disease?: A systematic review and meta-analysis, J Am Coll Cardiol, 2012, vol 60, pp 1828-37;
[5] Rahmim A en Zaidi H, PET versus SPECT: strengths, limitations and challenges, Nucl Med Commun, 2008, vol 29, pp 193-207;
[6] Senthamizhchelvan S, Bravo PE et al, Human biodistribution and radiation dosimetry of 82Rb, J Nucl Med, 2010, vol 51, pp 1592-9;
[7] Farhad H, Dunet V et al, Added prognostic value of myocardial blood flow quantitation in rubidium-82 positron emission tomography imaging, Eur Heart J Cardiovasc Imaging, 2013, vol 14, pp 1203-1210.